默沙东口服艾滋病双药疗法获FDA批准上市
当地时间4月21日,默沙东宣布,美国FDA已批准其每日一次口服双药疗法 Doravirine/Islatravir(DOR/ISL)上市,适用于已实现病毒学抑制(HIV-1 RNA 低于 50 拷贝/mL)、抗逆转录病毒治疗方案稳定、无病毒学治疗失败史且无已知与多拉韦林耐药相关的替代疗法的患者。

截图来源:默沙东官网
根据默沙东新闻稿,DOR/ISL是首个非整合酶抑制剂(INSTI)双药方案。其中,Islatravir是一种在研的核苷类逆转录酶易位抑制剂(NRTTI),它通过多种机制阻断 HIV-1复制,包括抑制逆转录酶易位,从而导致链终止;以及诱导病毒DNA结构改变,从而导致链终止延迟。
该药的另一成分Doravirine则是每日一次的口服创新非核苷逆转录酶抑制剂,通过与HIV-1病毒的逆转录酶结合,防止HIV-1病毒将RNA转化为DNA,从而阻断HIV-1病毒复制。此前,Doravirine已在全球多地被批准用于治疗HIV-1成人感染者,可与其他抗逆转录病毒药物联合使用,既可作为单一药物(Pifeltro),也可作为单片复方制剂(Delstrigo)的组成部分。
默沙东曾在新闻稿中表示:Islatravir 通过多种机制阻断HIV-1复制,包括逆转录酶易位抑制,有望成为一系列双药、非整合酶抑制剂的每日和每周治疗方案的核心药物。如果获得批准,DOR/ISL将成为我们产品组合中首个此类方案,并可能为满足HIV感染者不断变化的治疗需求提供重要的全新选择。
阿斯利康新一代TROP2 ADC在华上市
4月22日,阿斯利康与第一三共联合开发的新一代靶向TROP2抗体偶联药物(ADC)注射用德达博妥单抗 正式在中国商业上市,首批药品将陆续落地全国各大医院与药房,为中国HR阳性、HER2阴性晚期乳腺癌患者带来全新的精准治疗选择。这也是继恩美曲妥珠单抗后,双方合作引入中国市场的第二款ADC产品。
此前,德达博妥单抗已于2025年8月基于全球Ⅲ期TROPION-Breast01研究的积极结果,获国家药品监督管理局批准,适应症为既往接受过内分泌治疗且。在晚期疾病阶段接受过至少一线化疗的不可切除或转移性HR阳性、HER2阴性(IHC 0、IHC 1+或 IHC 2+/ISH-)乳腺癌成人患者。
全球Ⅲ期TROPION-Breast01研究数据显示,与化疗相比,德达博妥单抗可将患者疾病进展或死亡风险显著降低37%(HR=0.63,p<0.0001);针对83例中国患者的事后分析显示,德达博妥单抗组中位无进展生存期(PFS)达8.1个月,较化疗组的4.2个月实现翻倍,疾病进展或死亡风险降低46%(HR=0.54),展现出更贴合中国患者的临床获益。
先声药业乐德奇拜单抗收到通知件
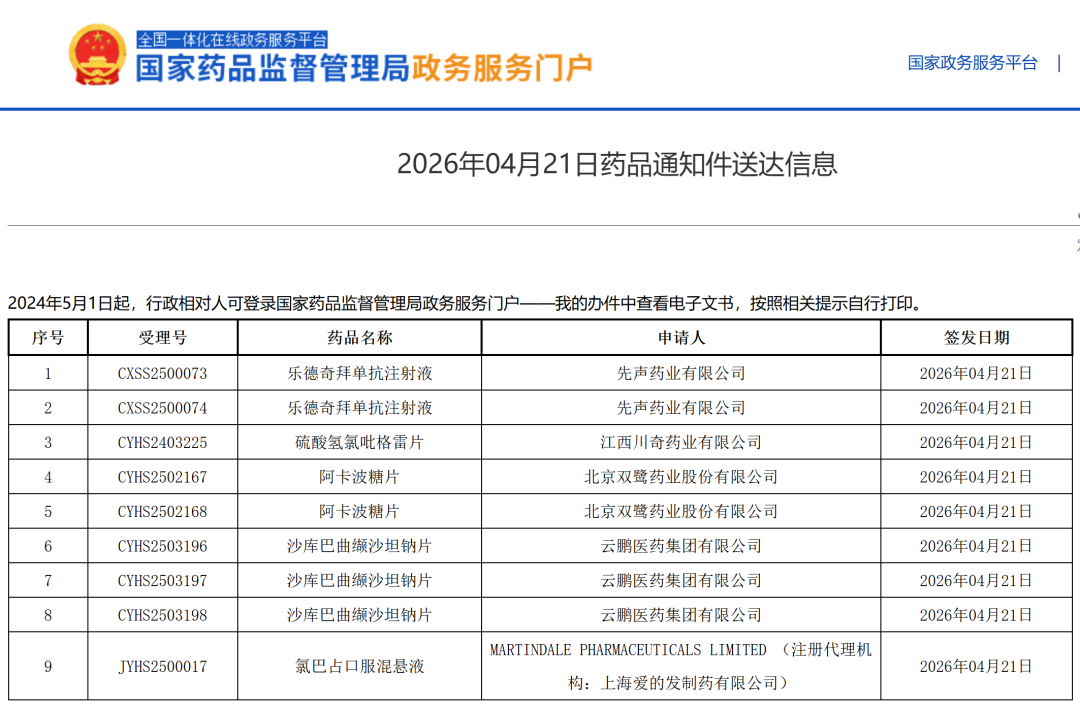
4月21日,国家药监局发布药品通知件送达信息,本批次共有9个受理号收到通知件,均为上市申请,其中先声药业申报的乐德奇拜单抗注射液收到通知件,原因未知,其申报的适应症为:用于治疗成人及青少年特应性皮炎。此前,2025年7月,先声药业宣布乐德奇拜单抗新药上市申请获国家药品监督管理局受理。
公开资料显示,乐德奇拜单抗是一种高效能的抗IL-4Rα单克隆抗体,其阻断由IL-4和IL-13诱导的IL-4Rα信号传导,抑制由IL-4和IL-13诱导的TF-1细胞增殖,具有起效更快、用药频率更低以及更高的临床反应率的潜在临床意义。
乐德奇拜单抗由香港康乃德生物医药有限公司研发,2023年11月,先声药业以1.5亿元人民币首付款+潜在最高8.75亿元人民币里程碑金额,以及最高两位数比例的销售分成,引进了乐德奇拜单抗的大中华区权益。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx