01
恒瑞抗癌联合疗法启动新Ⅲ期临床
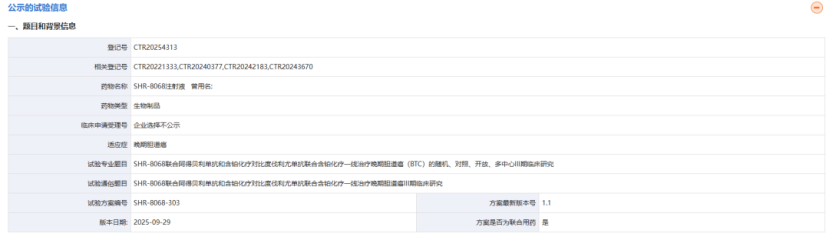 截图来源:药物临床试验登记与信息公示平台
截图来源:药物临床试验登记与信息公示平台这是一项随机、开放、对照、多中心Ⅲ期研究,旨在评价两种联合疗法用于晚期BTC患者一线治疗的有效性和安全性。该试验拟在国内入组604人,研究的主要终点指标是总生存期(OS)。
阿得贝利单抗注射液是恒瑞自主研发的人源化抗PD-L1单克隆抗体,已于2023年获批上市,获批适应症为与卡铂和依托泊苷联合用于广泛期小细胞肺癌患者的一线治疗。
SHR-8068(CS1002)是恒瑞以最高约13亿元从基石药业引进的一款全人源抗CTLA-4单克隆抗体,可增强抗肿瘤免疫效应。此前恒瑞已针对该药启动2项Ⅲ期临床试验,本次是启动的第3项Ⅲ期临床试验:
2025年9月,SHR-8068联合阿得贝利单抗及含铂化疗对比替雷利珠单抗联合含铂化疗一线治疗PD-L1表达阴性的局部晚期或转移性非小细胞肺癌;
2024年9月,SHR-8068联合阿得贝利单抗和贝伐珠单抗对比信迪利单抗联合贝伐珠单抗一线治疗晚期肝细胞癌。
02
百利天恒首款核药启动临床
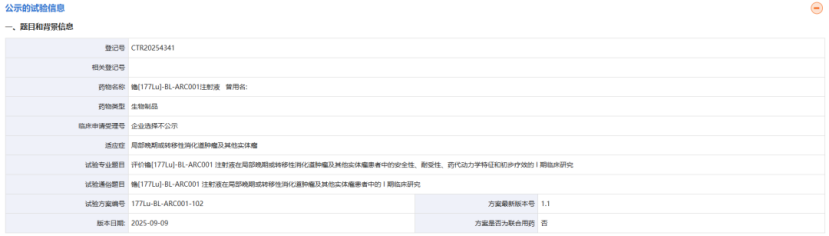 截图来源:药物临床试验登记与信息公示平台
截图来源:药物临床试验登记与信息公示平台
据介绍,这是一项评价镥[177Lu]-BL-ARC001注射液在局部晚期或转移性消化道肿瘤及其他实体瘤患者中的安全性、耐受性、药代动力学特征和初步疗效的Ⅰ期临床研究:
剂量递增阶段(Ia)的主要目的是观察 177Lu-BL-ARC001 在局部晚期或转移性实体瘤患者中的安全性和耐受性,从而确定最大耐受剂量(MTD) 和剂量限制性毒性(DLT);次要目的是评估 177Lu-BL-ARC001 的药代动力学特征、免疫原性和全身分布;估算 177Lu-BL-ARC001 的辐射剂量,和毒性相关的辐射剂量。
扩大入组阶段(Ib)的主要目的是进一步观察 177Lu-BL-ARC001 在 Ia 期推荐剂量下的安全性和耐受性,确定 RP2D;次要目的是评估 177Lu-BL-ARC001 的初步疗效、药代动力学特征、免疫原性和全身分布;估算177Lu-BL-ARC001的辐射剂量,和毒性相关的辐射剂量。
177Lu-BL-ARC001是百利天恒基于其自主研发的HIRE-ARC平台在抗体放射性核素偶联药物(ARC)领域的首款Ⅰ1类创新药物,同时也是其拥有完全自主知识产权的潜在全球首创(First-in-class)的ARC药物。
177Lu-BL-ARC001通过抗体介导的精准靶向递送技术及放射性核素强大的肿瘤杀伤能力,与传统放射性核素偶联药物相比,具有更强的靶点特异性、更高的肿瘤富集性,并有望展现出更好的抗耐药性。
03
信达生物1类新药启动一项Ⅱ/Ⅲ期临床
11月3日,药物临床试验登记与信息公示平台官网显示,信达生物登记了一项多中心、随机、双盲、安慰剂对照的Ⅱ/Ⅲ期临床研究,以评估匹康奇拜单抗治疗活动性银屑病关节炎患者的有效性和安全性。
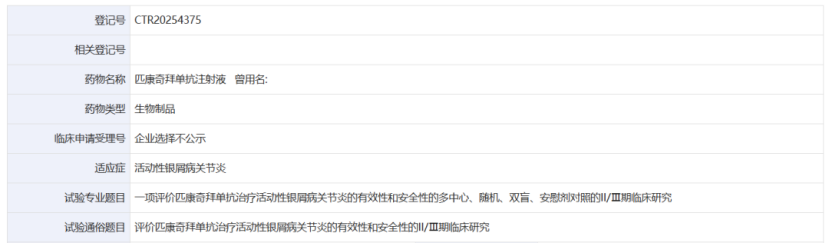 截图来源:药物临床试验登记与信息公示平台
截图来源:药物临床试验登记与信息公示平台
公开资料显示,匹康奇拜单抗(IBI112)是信达生物自主研发的一款重组抗白介素 23p19 亚基(IL-23p19)抗体注射液。该药可特异性结合 IL-23p19 亚基,通过阻止 IL-23 与细胞表面受体结合,阻断 IL-23 受体介导信号通路发挥抗炎作用。
2024年9月,匹康奇拜单抗的首个上市申请获NMPA受理,用于治疗中重度斑块状银屑病,是首个报上市的国产IL-23p19单抗。
本次启动的是一项Ⅱ/Ⅲ期临床研究(CTR20254375),试验目的是评价匹康奇拜单抗治疗活动性银屑病关节炎改善症状和体征的有效性。试验药物为匹康奇拜单抗注射剂(预充式自动注射笔),皮下注射,每次给药 200 mg,采用多次给药方式,给药至 44 周。研究将在国内 65 个医疗机构开展,计划入组 222 例患者。
除了斑块状银屑病、活动性银屑病关节炎,信达还在开展匹康奇拜单抗治疗溃疡性结肠炎的Ⅱ期临床。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx