 截图来源:CDE官网
截图来源:CDE官网
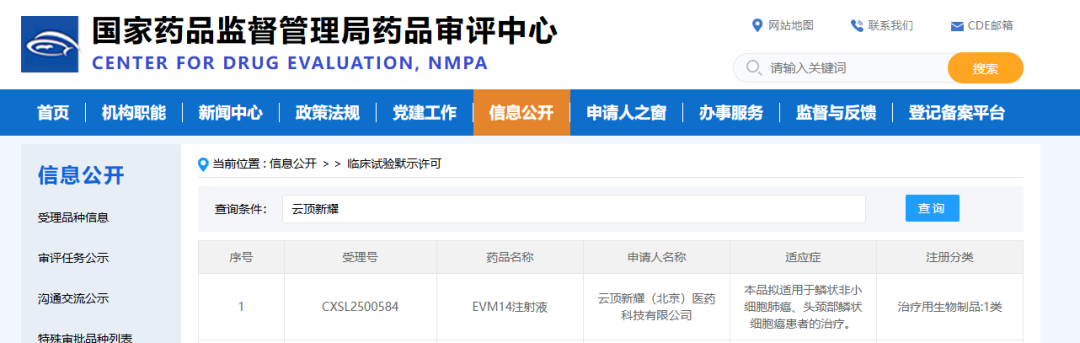
公开资料显示,EVM14基于云顶新耀自主知识产权的mRNA技术平台研发,是一款靶向5个TAA的通用现货型肿瘤治疗性疫苗,拟用于治疗多种鳞状细胞癌,包括非小细胞肺鳞癌(sq-NSCLC)和头颈部鳞状细胞癌(HNSCC)。
此前,EVM14新药临床试验申请于2025年3月获FDA批准。此次获批的I期临床试验主要目的是观察EVM14的安全性和耐受性,次要目的是观察其疗效。在EVM14 I期临床试验探索的瘤种中,大多数患者会表达5个TAA之一。其中,约96%的sq-NSCLC患者和97%的HNSCC患者检测到至少一个TAA基因的表达。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx