来源:药渡
2025年8月5日,中国国家药监局药品审评中心(CDE)官网显示,石药集团以化药注册分类2.2类申报的司美格鲁肽注射液上市申请已获得受理。
这一消息标志着石药集团在GLP-1受体激动剂领域的研发取得了重要进展,将为国内2型糖尿病患者和超重/肥胖患者带来了新的治疗选择。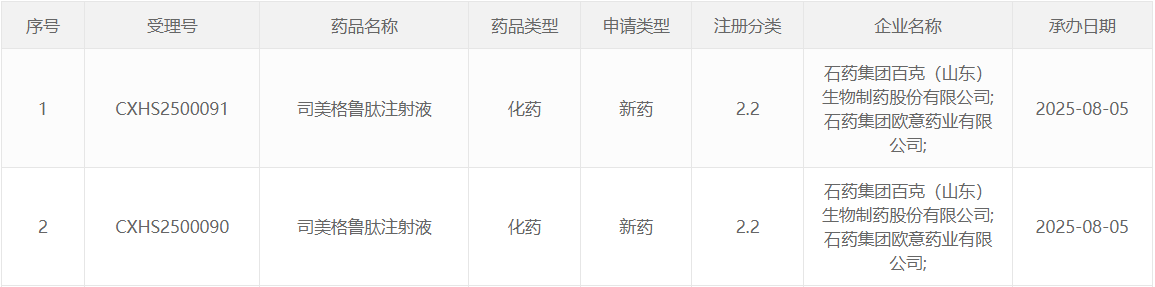 图1. 石药司美格鲁肽申报上市获受理,来源:CDE官网
图1. 石药司美格鲁肽申报上市获受理,来源:CDE官网
司美格鲁肽是一种长效GLP-1受体激动剂,原研由诺和诺德开发,广泛应用于2型糖尿病和减重治疗。近年来,随着GLP-1类药物在代谢性疾病治疗中的优势逐渐显现,国内药企纷纷布局相关产品的研发。石药集团此次申报上市的司美格鲁肽注射液,不仅为国内患者提供了更多潜在的治疗选择,也进一步加剧了国内GLP-1市场的竞争。
石药集团开发的司美格鲁肽注射液使用的原料完全通过化学合成法制备,制备出的原料纯度更高,避免了生物发酵过程引入的宿主蛋白等免疫原性物质,并保证了杂质水平不高于DNA重组技术制备的司美格鲁肽。临床前研究结果显示,该产品与DNA重组技术制备的司美格鲁肽注射液具有相似的生物活性和减重效果、体内降糖效果。
2024年8月和9月,该产品先后在中国完成治疗2型糖尿病和用于体重管理的3期临床试验全部受试者入组。此外,石药集团还在开发GLP-1受体激动剂司美格鲁肽长效注射液(SYH9017),为每月一次给药的司美格鲁肽制剂。该产品是一种长效缓释制剂,旨在实现每月一次给药。
司美格鲁肽原研由诺和诺德开发,2024年销售额为292.96亿美元,其中减重版Wegovy为84.48亿美元,同比增长86%。国产司美格鲁肽的研发和上市进程正在加速,目前已有20多款司美格鲁肽进入临床阶段,其中6款产品已申报上市,分别来自九源基因、丽珠集团、齐鲁制药、联邦制药、中美华东和石药集团。
从注册分类来看,齐鲁制药和石药集团的司美格鲁肽是按照化药改良新药2.2类申报的,九源基因、丽珠集团、联邦制药和中美华东都是按照生物类似药3.3类申报的。据预测,国产司美格鲁肽最早有望在今年第三季度获批上市,首个或许会在九源基因和齐鲁制药中产生。
石药集团司美格鲁肽注射液的上市,将为国内2型糖尿病患者和超重/肥胖患者提供更多的治疗选择。与原研产品相比,该产品在纯度和安全性上具有潜在优势,有望为患者带来更好的治疗体验。
随着石药集团司美格鲁肽注射液的申报上市,国内GLP-1市场竞争将进一步加剧。目前,国内已有多个司美格鲁肽仿制药/改良新药进入临床和申报阶段,预计未来几年将有多款产品陆续获批。石药集团凭借其在化学合成法方面的技术优势,有望在市场竞争中占据一席之地。
石药集团在GLP-1领域的布局不仅限于司美格鲁肽注射液,其长效注射液SYH9017的研发也在稳步推进。该产品每月一次给药的便利性,有望进一步提升患者的治疗依从性。此外,石药集团还将在减重和心血管疾病风险降低等领域继续探索司美格鲁肽的潜力。
总之,石药集团司美格鲁肽注射液的申报上市,为国内GLP-1市场注入了新的活力。随着更多国产司美格鲁肽产品的获批上市,国内GLP-1市场将迎来更激烈的竞争,同时也将为患者带来更多更好的治疗选择。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx