在明年1月1日即将正式实施的新医保目录中,罕见病药物得到了越来越多的市场关注。
在前不久国家医疗保障局发布《2023年国家基本医疗保险、工伤保险和生育保险药品目录》中,15款罕见病药物谈判/竞价成功进入医保,数量创近三年新高,填补10个病种的用药保障空白。
一直以来,罕见病是世界性的医学难题,也是全球共同的重大公共卫生问题。罕见病的“罕见”特点,导致误诊或者延误诊断情况多发,因误诊误治使患者误用药,给患者带来额外的身体、心理、经济等方面负担。
另一方面,由于许多罕见病发病机制不明、缺乏研究,以及患者群体数量少导致的临床推进难度大。这也加剧了相关治疗药物的不多,且价格昂贵的市场困境。加之很多罕见病属于终身性疾病,患者需要终生用药,罕见病药物的可及性和可支付性方面也是困扰罕见病患者群体的一大难题。
值得关注的是,据国家医保局介绍,针对罕见病患者“有药买不起”的痛点,坚持多措并举,在准入条件上连续三年取消罕见病用药的获批年限限制,在评审、测算等环节,明确予以倾斜,支持符合条件的罕见病用药优先纳入医保。
聚焦临床需求“孤儿药”加速进入医保随着罕见病药物利好政策的频频出台,加上罕见病领域未被满足的需求大、市场竞争小等特点,越来越多的本土药企加码布局罕见病领域。一些曾经“无药可治”的罕见病,患者或能在与时间的赛跑中等来“救命良药”。
近年来,医保药品目录建立了“每年一调”的动态调整机制,将准入方式由专家遴选制改为企业申报制,申报范围主要聚焦5年内新上市药品。目前,5年内新上市药品在当年新增品种中的占比从2019年的32%提高至2023年的97.6%。
从数据上看,2023年有57个品种实现“当年获批、当年纳入目录”。加之,在国家医保局“在准入条件上连续三年取消罕见病用药的获批年限限制”的支持下,不少“踩点”获批的罕见病药品也加速进入了2023医保目录。
其中,来自再鼎医药的创新药艾加莫德α注射液,用于治疗成人全身型重症肌无力(gMG)患者。据了解,全球约有70万名重症肌无力患者,其中,国内的患者就约有20万名。该疾病是一种罕见的慢性自身免疫性疾病,患者一般表现出极度疲劳和面部表情、言语、吞咽和活动困难。这款产品仅仅在2023年6月刚获批,便成功通过谈判进入医保。这也重症肌无力等多项病症群体多年来未得到解决的迫切局面。
另一款来自琅铧医药的盐酸替洛利生片,也是在今年6月30日“踩点获批”,中国国家药品监督管理局才正式批准盐酸替洛利生片(铧可思)用于治疗发作性睡病成人患者的日间过度嗜睡或猝倒。其适应症更是刚刚被收入今年新发布的《第二批罕见病目录》,在共同努力下,患者在2024年就能用到“医保药”似乎显得更幸运一些。
此外,发作性睡病、泛发性脓疱型银屑病、婴儿痉挛症、胃肠道间质瘤这几个病种今年9月刚被纳入第二批《罕见病目录》,这些疾病相关的治疗药物也顺利通过医保谈判被纳入医保。
在罕见病领域,不可忽视跨国药企一直以来都是这一领域的重要参与者。2023年医保谈判,勃林格殷格翰(BI)、阿斯利康、百时美施贵宝(BMS )、罗氏等企业均有罕见病药品进入医保。
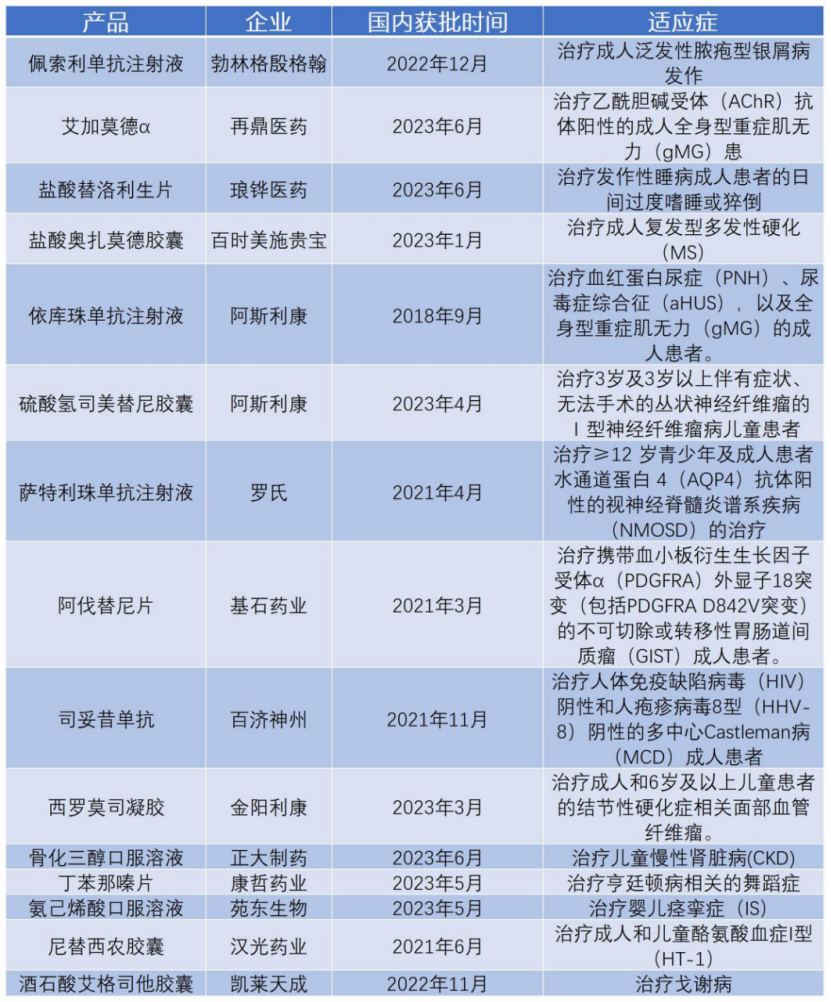
具体来看,勃林格殷格翰带来“佩索利单抗注射液”,用于治疗“成人泛发性脓疱型银屑病(GPP)”、百时美施贵宝的“盐酸奥扎莫德胶囊”,适应症为“成人复发型多发性硬化”、罗氏的“萨特利珠单抗注射液”,用于治疗“视神经脊髓炎谱系疾病(NMOSD)”。
以及阿斯利康在2023年带来了两款罕见病治疗产品,一款是阿斯利康和默沙东共同开发的“硫酸氢司美替尼胶囊”,另一款则是“依库珠单抗注射液”。前者刚在今年4月28日在国内获批用于治疗“I型神经纤维瘤病(NF1)儿童患者”,是国内首个且唯一获批的Ⅰ型神经纤维瘤病治疗药物,后者则拥有3项适应症:血红蛋白尿症(PNH)、尿毒症综合征(aHUS),以及全身型重症肌无力(gMG)的成人患者。
在上述产品之外,还有包括百济神州、基石药业、康哲维盛、汉光药业等在内的多家国内企业,带来它们的罕见病用药。
从申报单位看,本次谈判成功的15种药物中,来自跨国药企的有6种、本土企业的有10种。反映出了已经有更多本土药企在致力于罕见病药物的引进和研发,医疗和科研机构也陆续加入攻克罕见病药物研发难题的队伍中。
总体来看,本次谈判成功的罕见病药品中,包括艾加莫德α注射液在内,共有9种药品的上市时间不足一年。也体现出了国家对需求巨大的临床空白产品的支持。
支付端多措并举缓解临床诊疗难题2018年5月,国家发布了《第一批罕见病目录》(收录121种罕见病),自此以来,有关部门也开展了一系列关于罕见病诊疗到药物研发及上市、医疗保障等多方面的政策支持。
2023年9月,业内期待已久的《第二批罕见病目录》公布,纳入85种罕见病。截至目前,合计有207种罕见病被收入目录。时隔五年,第二批罕见病目录的公布,是我国罕见病领域的又一里程碑事件。
另一方面,近年来,国家医保局通过优化准入程序,及时将符合条件的罕见病用药纳入医保药品目录,2023年国家医保药品目录调整工作方案对罕见病用药的申报条件未设置上市时间限制,纳入国家鼓励仿制药品目录的药品可以申报当年医保目录,进一步拓宽罕见病用药的准入范围。
反馈到本次医保谈判,来自凯莱天成的艾格司他仿制药物酒石酸艾格司他胶囊,可治疗一款“超罕”种类的I型戈谢病(GD1)成年患者的药品。这款国产首仿药酒石酸艾格司他胶囊纳入国家医保目录,在实现了零的突破的同时,定价几乎只有国外相同通用名产品的1/10。
有业内观点分析,虽然具体价格还未揭晓,但就该品种为代表进行分析,进入国产仿制药时代后,患者年负担已经低至10万元左右,再按医保乙类报销后,患者自费部分应该降到了几万元水平,极大降低了患者的负担。
如果对医保目录新增的15款罕见病用药的属性加以分类,会发现除了酒石酸艾格司他胶囊在内,氨己烯酸口服溶液用散、丁苯那嗪片、骨化三醇口服溶液等药物都是仿制药身份,比例约占到三分之一。
另一方面,据国家医保局今年8月披露的数据显示,通过医保目录准入谈判,已累计将26种罕见病用药纳入医保药品目录,平均降价超50%。叠加其他药品准入方式,截至上述时间点,在我国获批上市的75种罕见病用药已有50余种纳入医保药品目录。
针对谈判药品“进得了医保,进不了医院”难题,我国也已经建立起了谈判药品配备和支付的“双通道”机制,通过定点医疗机构和定点零售药店两个渠道,打通患者用药“最后一公里”。根据国家医保局发布的数据显示,截至2023年10月底,2022年版药品目录协议期内谈判药品已在全国23.92万家定点医疗机构配备。
可以说,本次《2023目录》从可及性和可支付性方面共同发力,以及创新产品的剂型突破,让患者用药依从性也有所提升,多维度缓解罕见病患者群体的用药难题。
