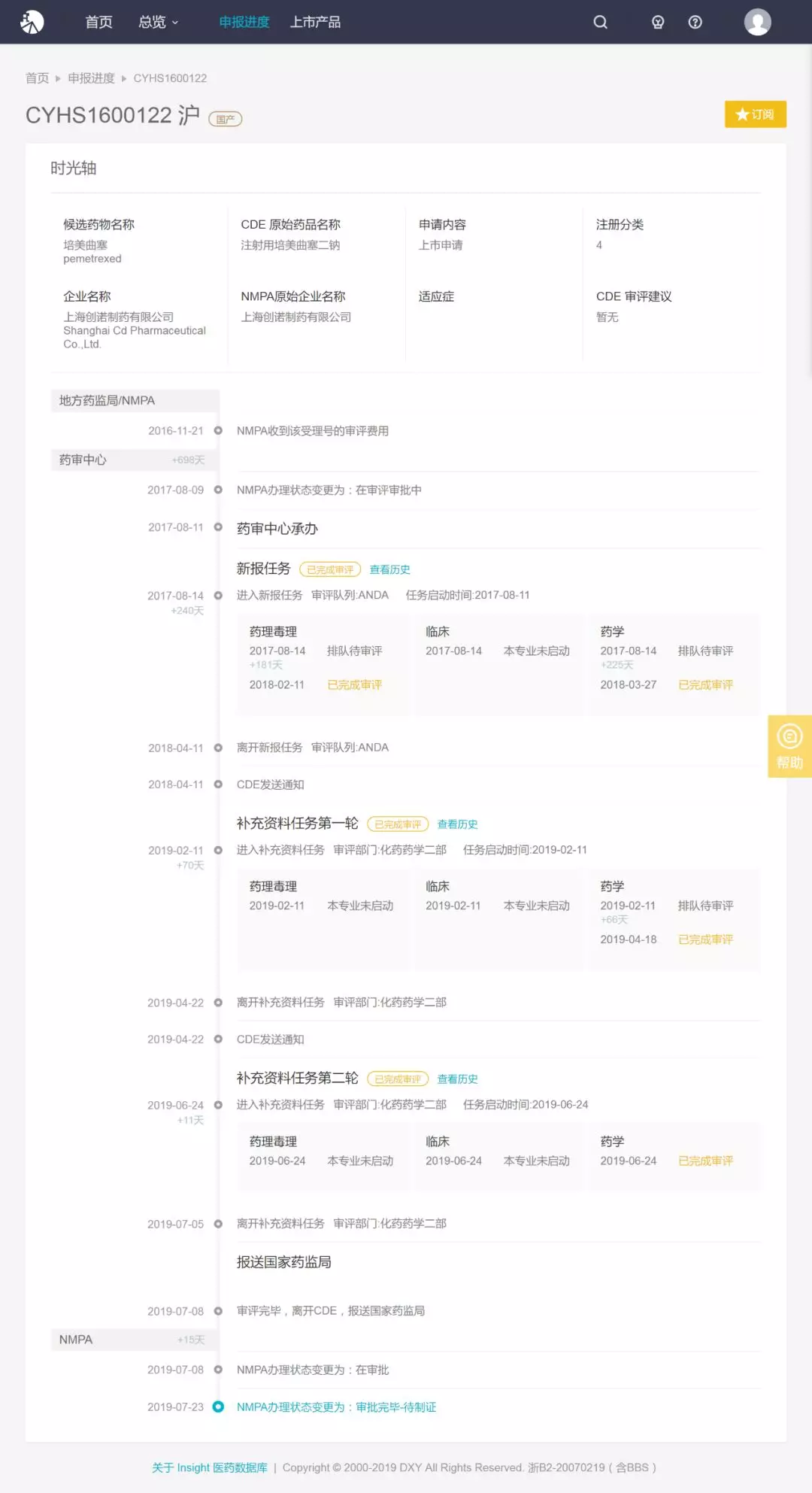
7 月 23 日,上海创诺制药的注射用培美曲塞二钠(CYHS1600122)的状态变更为「审批完毕-待制证」,该药为新 4 类申报,按照国家相关政策,获批上市后视同通过了一致性评价,也就是说上海创诺将有望成为第 2 家通过一致性评价的企业。
原研 4+7 未中选,狂降 30%
注射用培美曲塞(Alimta )是临床常用的肺癌化疗药,也是礼来最畅销的产品之一,该药属于抗代谢类药物,通过破坏细胞内叶酸依赖性的正常代谢过程,抑制细胞复制,从而抑制肿瘤增长。
注射用培美曲塞二钠为 4+7 带量采购品种,中选企业为四川汇宇,以 810 元/支(100 mg)和 2776.97 元/支(500 mg) 中标。
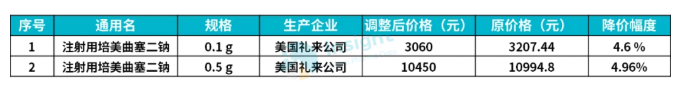
今年 3 月 4 日,浙江省药械采购中心发布公告显示,礼来主动申请下调其在浙江省注射用培美曲塞二钠的价格,礼来两种规格的注射用培美曲塞二钠价格分别由原来的 3207.44 元/盒,10994.80 元/盒,调整为 3060 元/支和 10450 元/支,降幅 4.96%。
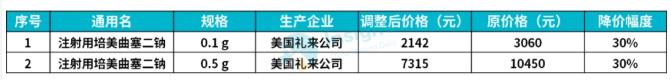
今年 7 月 19 日,黑龙江省药品集中采购网和贵州省药品集中采购工作同时发布了礼来注射用培美曲塞二钠的降价消息,根据两地的公告,礼来两种规格的注射用培美曲塞二钠价格调整为 2142.00 元/盒,7315.00 元/盒,整体降价幅度均为 30%,不过礼来降价之后,两个不同规格注射用培美曲塞的价格仍是四川汇宇的 2.6 倍左右。
21 亿大品种,14 个仿制药获批
2002 年 2 月,礼来培美曲塞以孤儿药身份被 FDA 批准与顺铂联用治疗恶性胸膜间皮瘤,随后于 2004 年 2 月被 FDA 批准与顺铂联用治疗恶性胸膜间皮瘤,2008 年 9 月,FDA 又批准了培美曲塞作为局部晚期肺癌或转移性非小细胞肺癌的一线治疗。即便专利过期,2018 年的全球销售额仍达到 21.33 亿美元。
2005 年 12 月该药在中国上市,被批准用于治疗恶性胸膜间皮瘤。Insight 数据库显示,国产注射用培美曲塞二钠有效批文共 28 个,14 家国产药企仿制,竞争较为激烈。
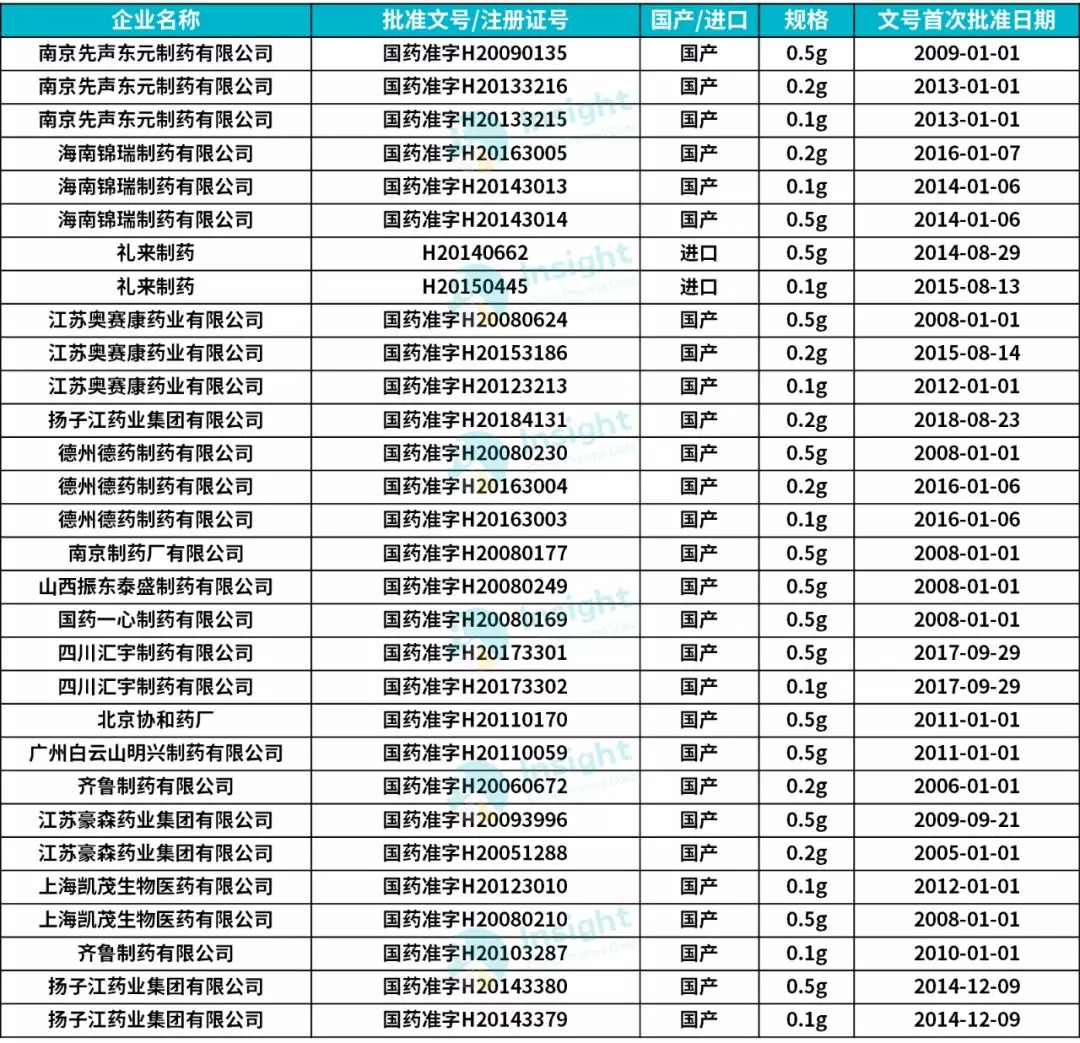
据了解,目前国内市场上,江苏豪森以 40% 的比例占据首位,齐鲁紧随其后,以 32% 的市场份额位列第二,原研礼来仅以 15% 屈居第三。
过评企业有望达到 5 家
上海创诺制药的注射用培美曲塞二钠获批上市后,即视同通过了一致性评价,将加入带量采购大潮,和原 4+7 中标企业四川汇宇制药同台竞争。
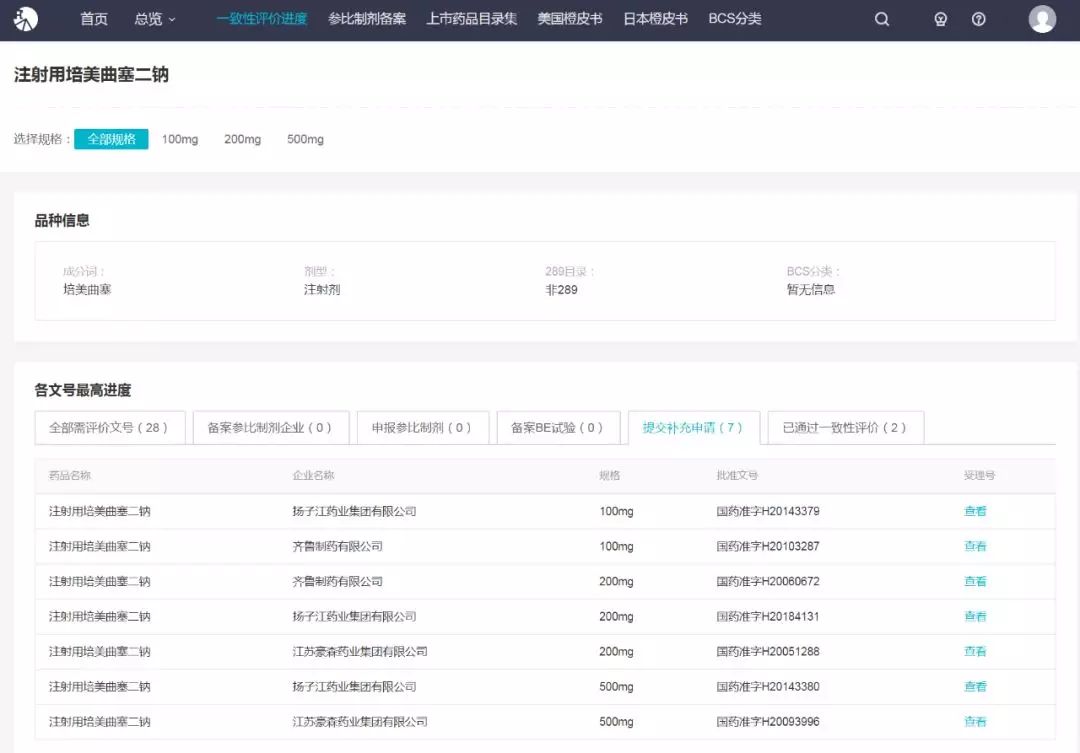
Insight 一致性评价库查询显示,目前在培美曲塞二钠已获批的 14 家国产仿制企业中,扬子江药业、齐鲁药业和豪森药业 3 家已经提交一致性评价补充申请(涉及 7 个批准文号),目前都处在新报任务在审。
同时,值得注意的是,上海创诺的培美曲塞二钠原料药上市申请也正在审评中,齐鲁制药也拥有培美曲塞二钠原料药批准文号,在 4+7 时代,原料药制剂一体化企业更能抵御降价压力,容易存活下来。
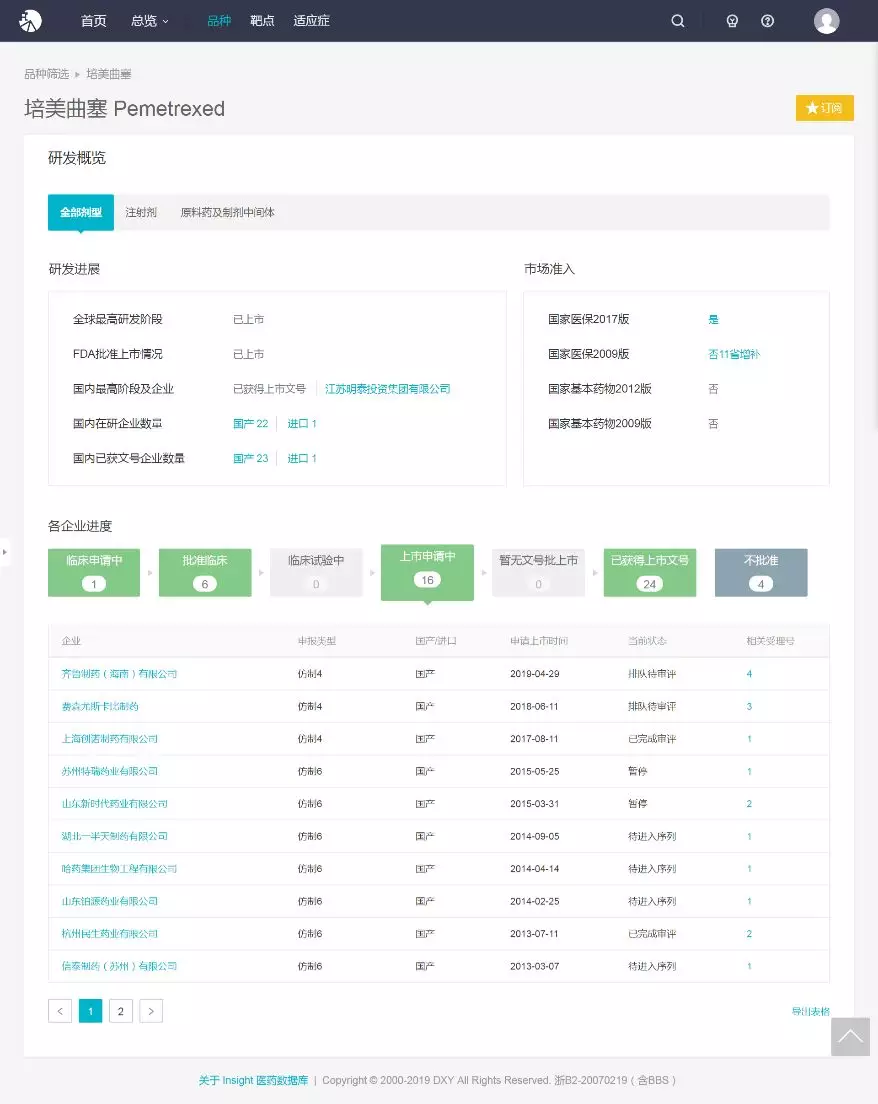
同时查询 Insight 申报进度数据库显示,目前国内有 15 家国产药企申报上市,其中有 13 家国产药企以仿制药 6 类申报上市,即使获批上市,后续仍需要申报一致性评价补充申请。
而费森尤斯卡比、齐鲁制药(预计为新规格报产)按照新 4 类申报上市,这两家获批后和上海创诺一样视同通过一致性评价,可以拿到 4+7 带量采购入场门票。但就两家企业受理号目前的审评状态来看,今年很难获批上市。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx