2018仿制药一致性评价展望
国君医药杨松/丁丹/于嘉轩
前言
国泰君安医药团队是全市场研究一致性评价最深入的团队,持续引领全市场一致性评价研究,我们从2016年上半年至今已经在:一致性评价政策、开展流程、企业进展、品种格局变化、鼓励评价开展政策、招标采购政策等多个领域发布47篇深度研究报告。本次我们再次发布110页深度专题展望报告,未来我们将继续在招标、采购、医保、使用等多个环节开展深度研究跟踪,敬请关注!
投资要点
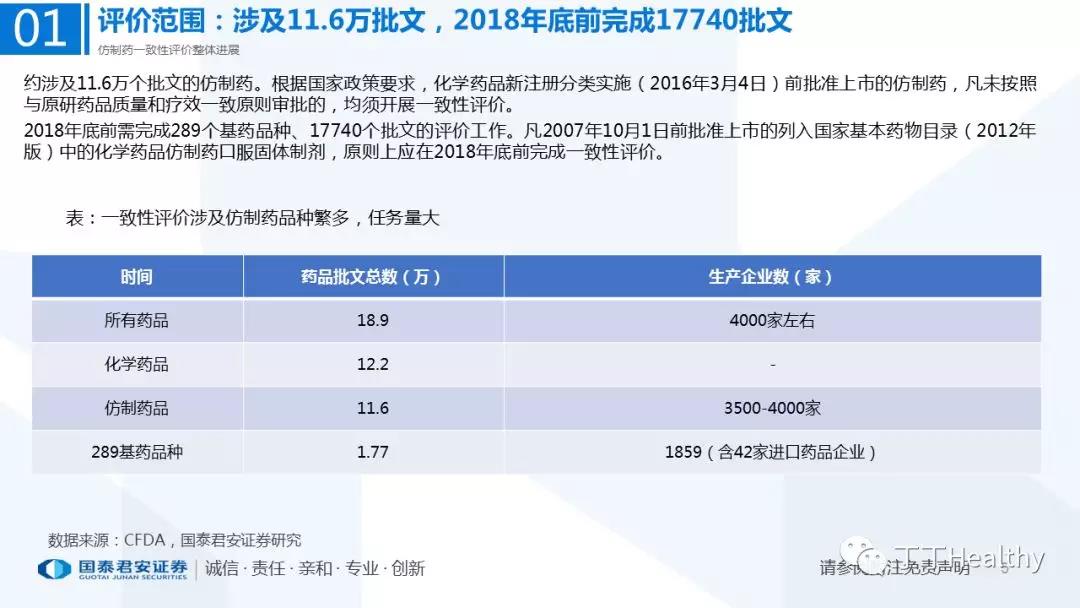
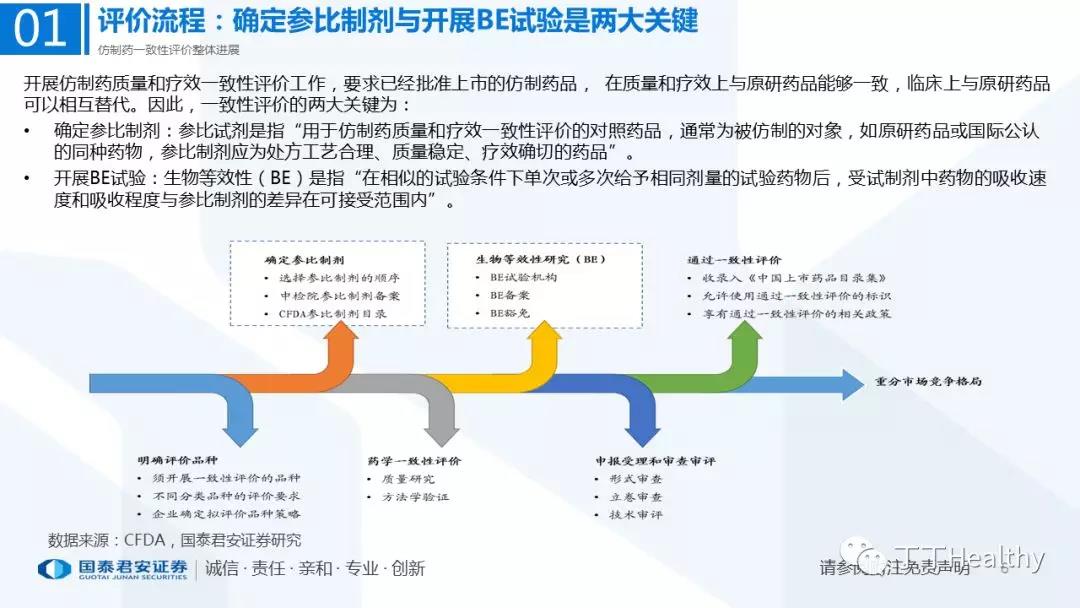
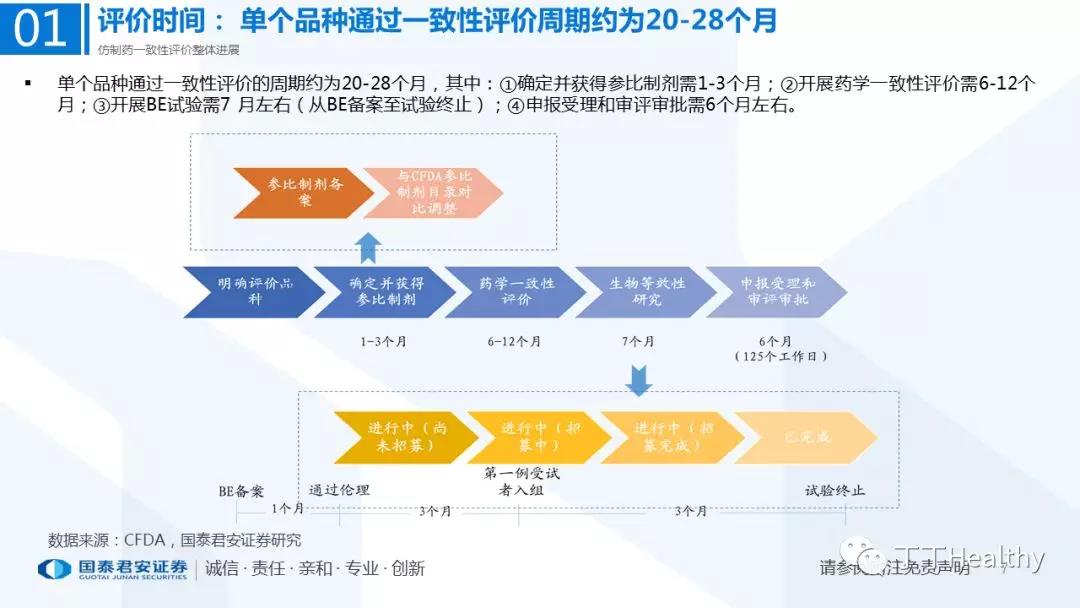
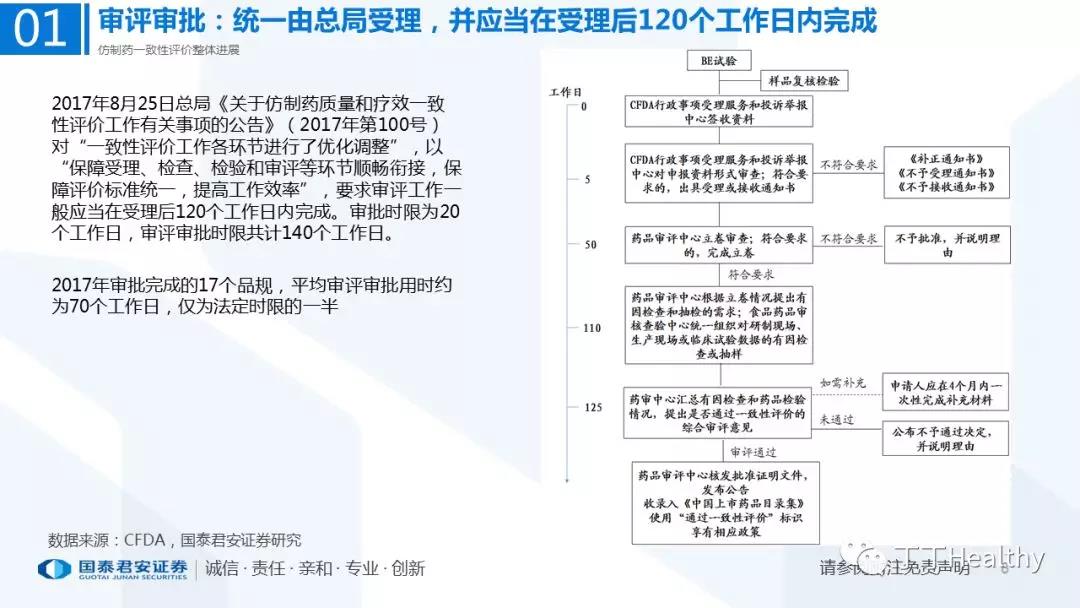
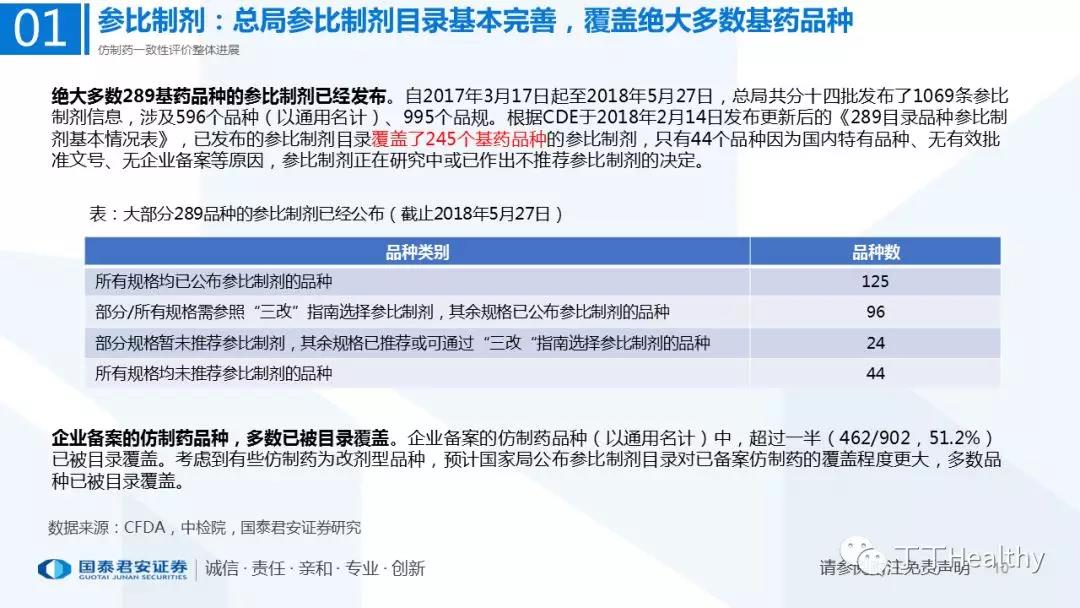
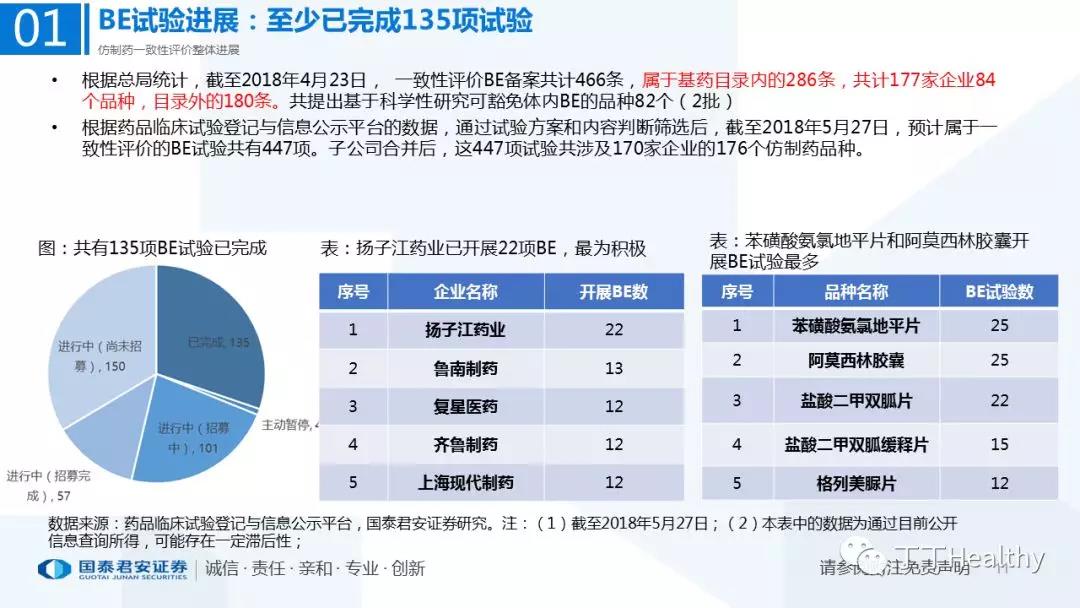
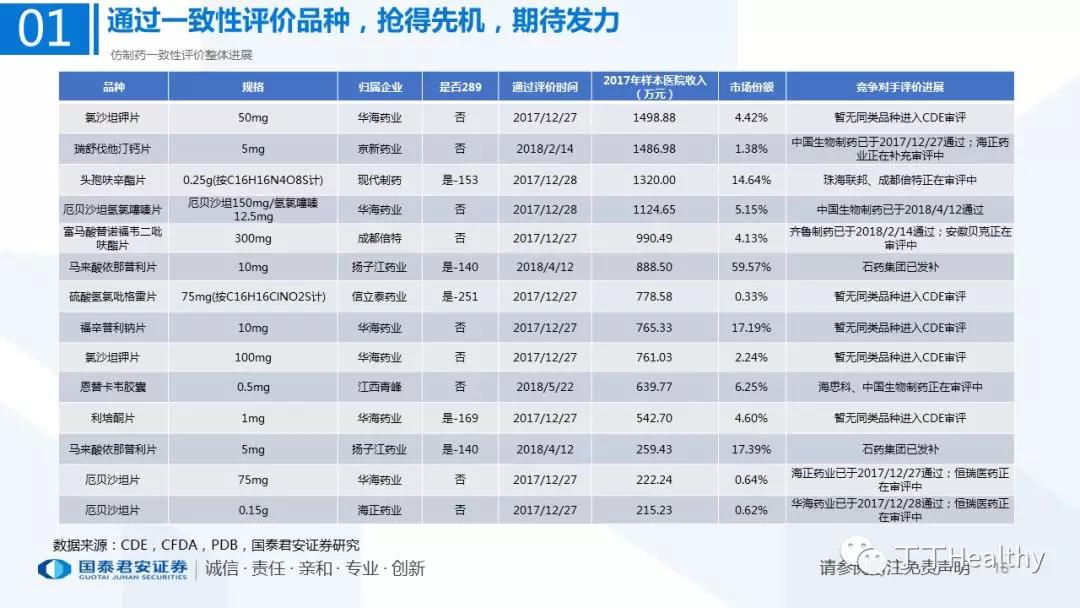
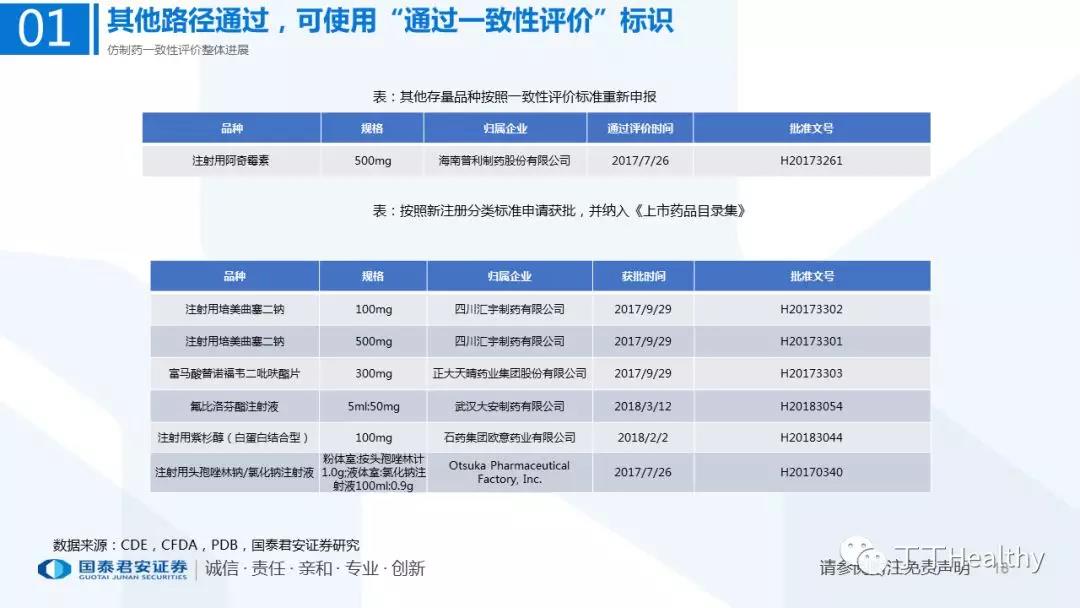
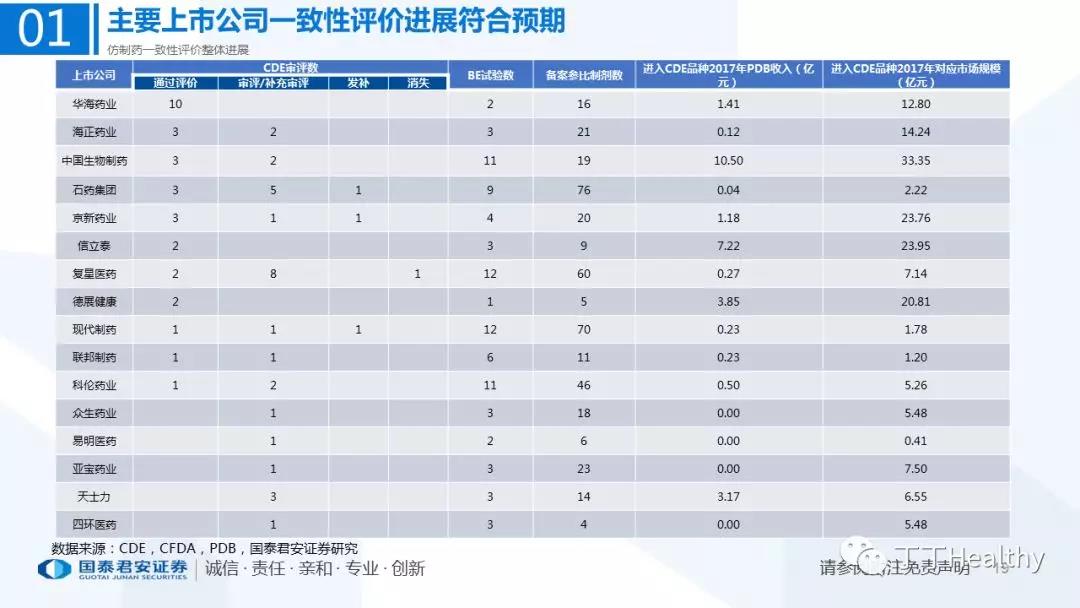
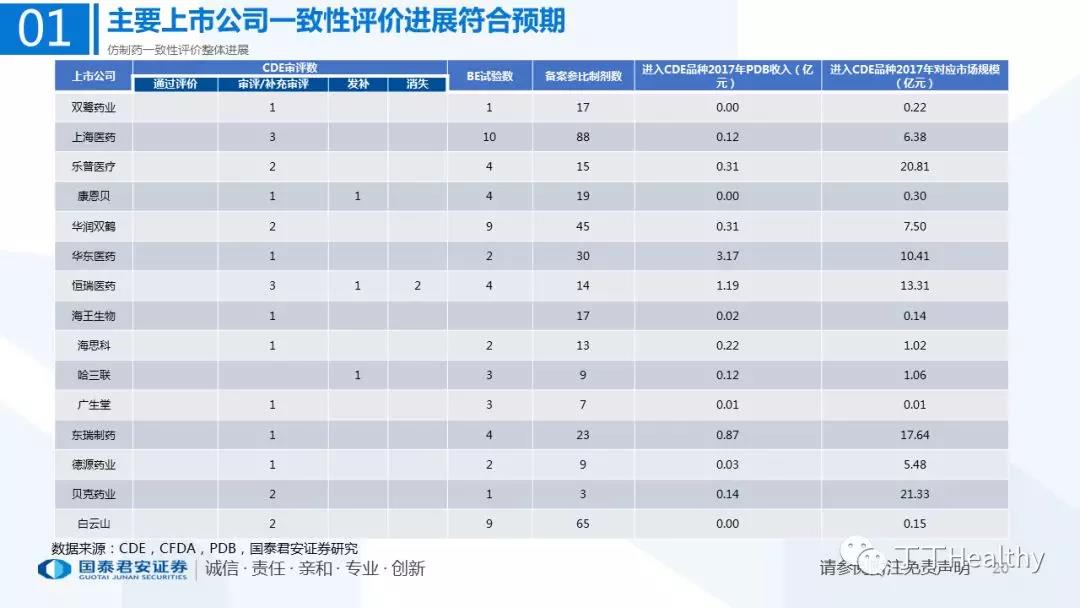
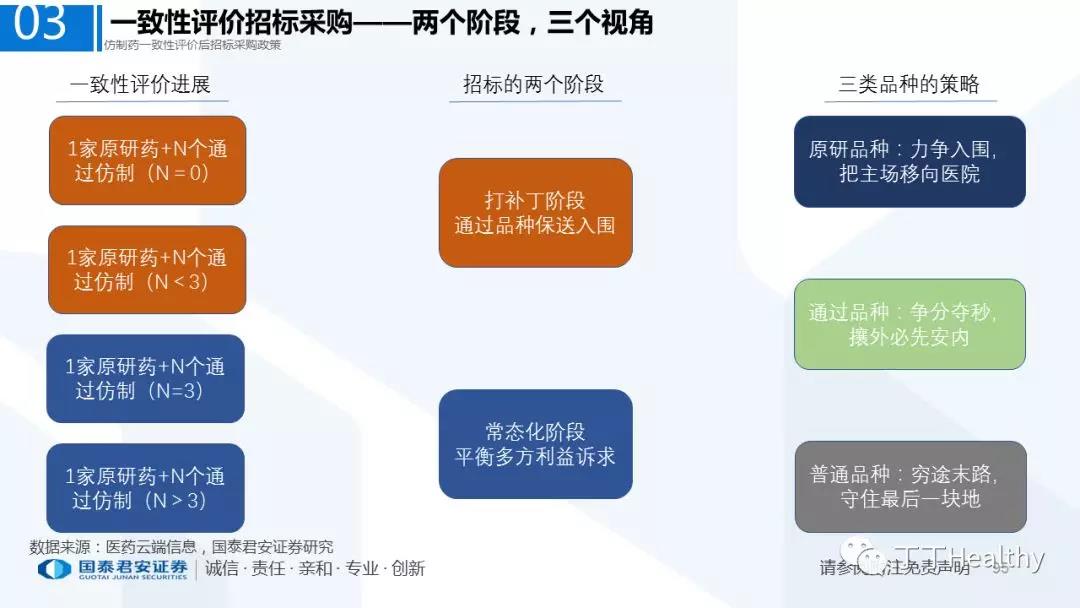
1.整体评价进展顺利,下半年获批节奏加速
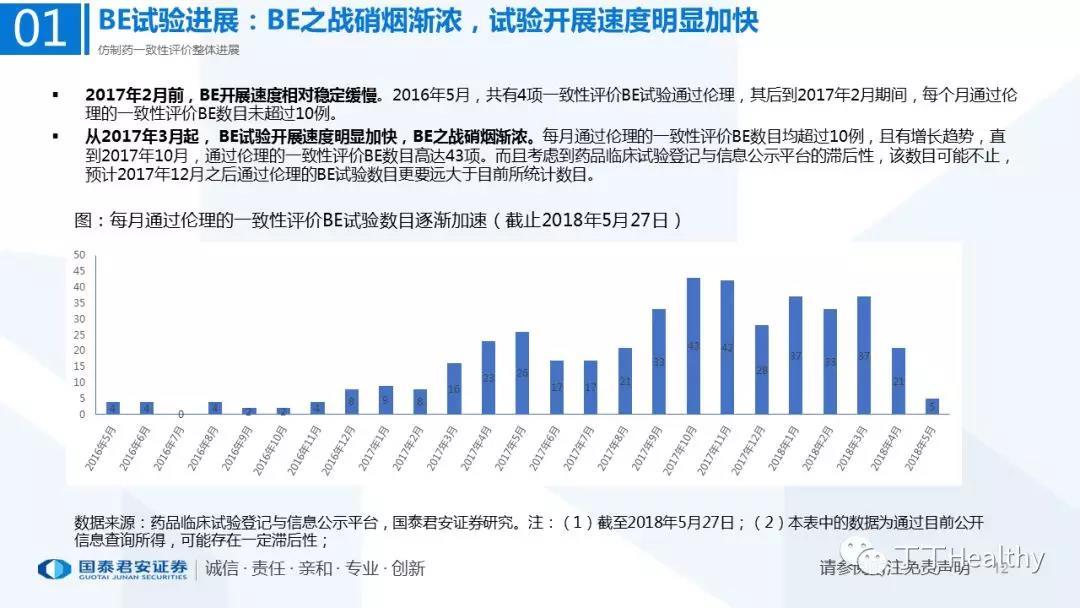
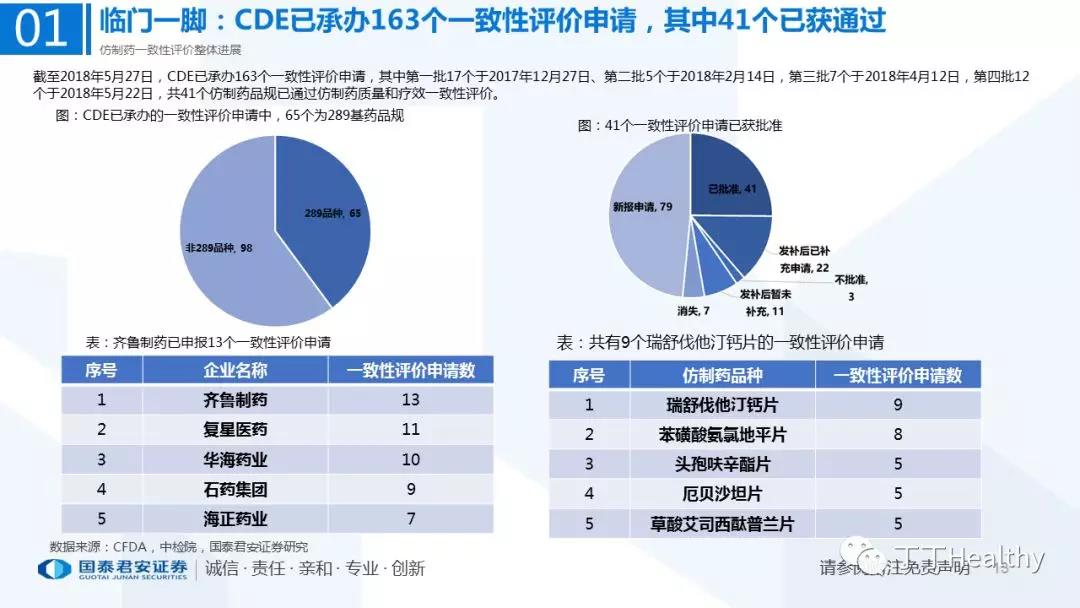
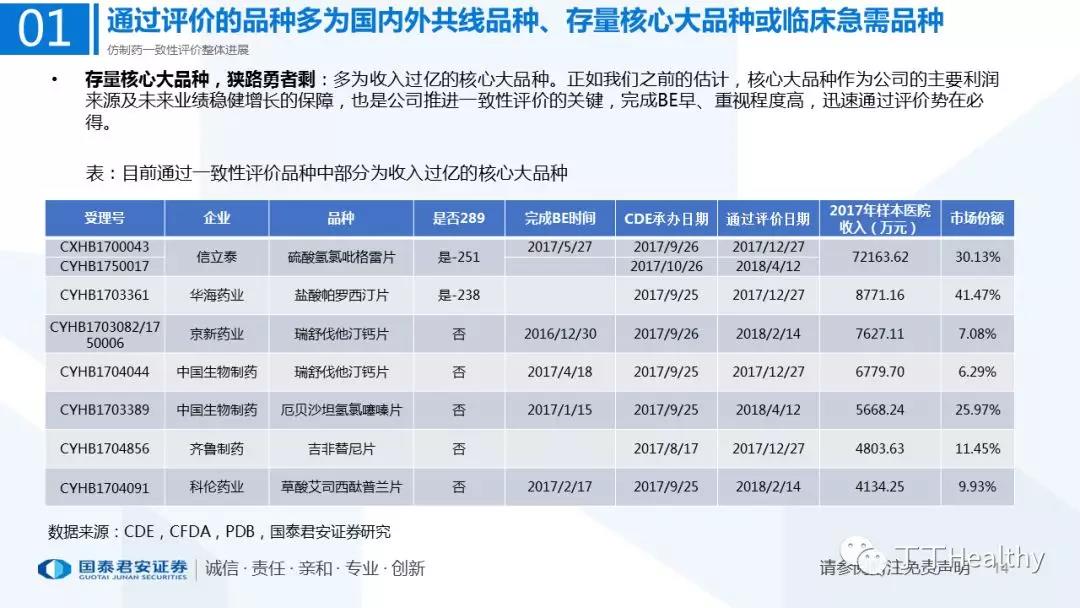
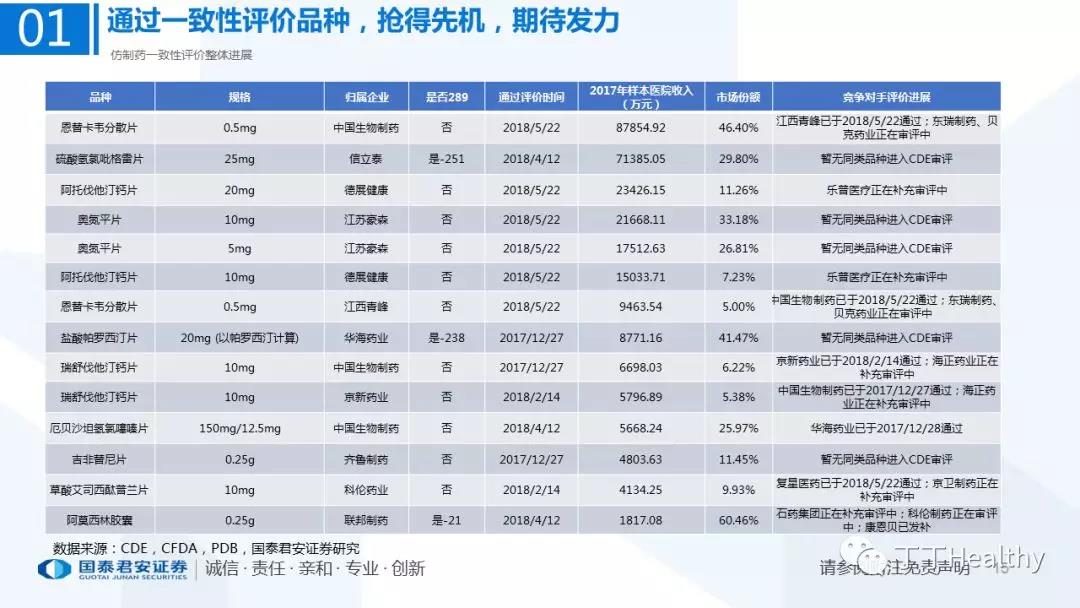
目前一致性评价通过品种已发布四批共计41个仿制药品规,从参比制剂备案、BE试验进展、CDE审评审批节奏看,2018年下半年获批节奏将加速。
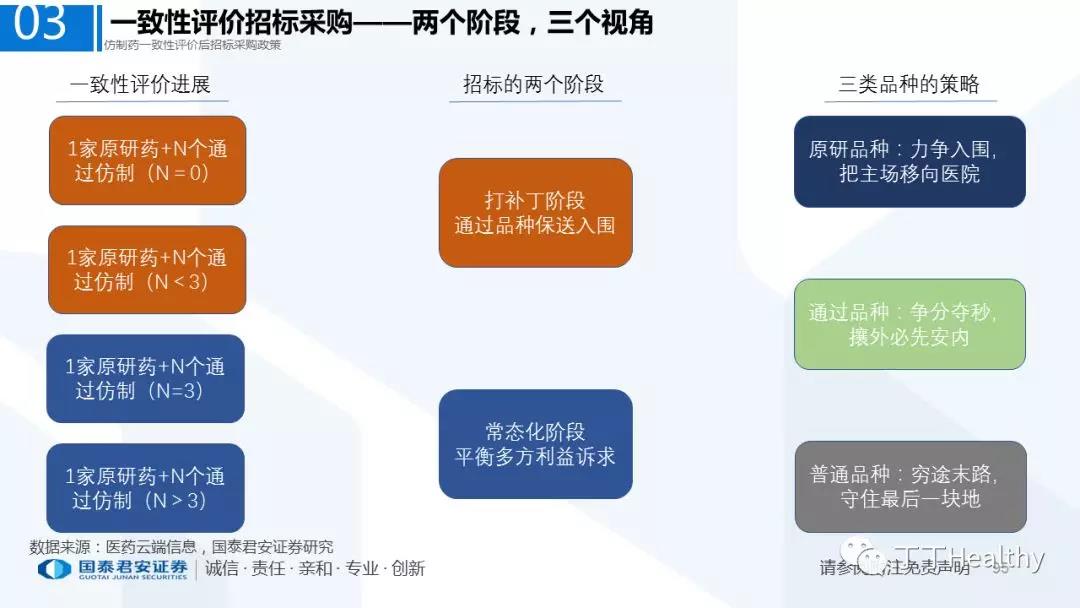
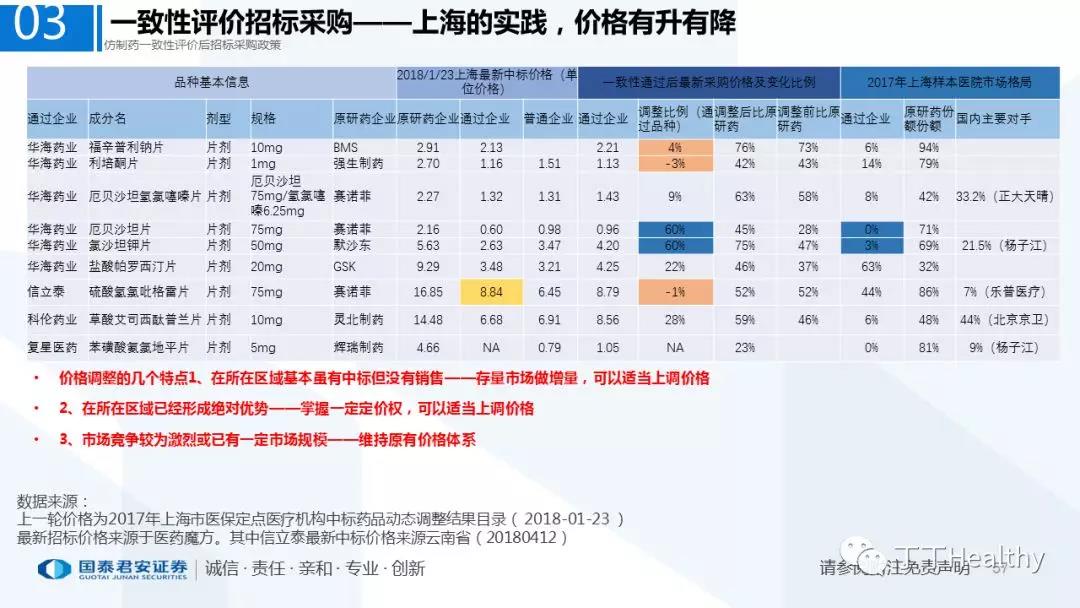
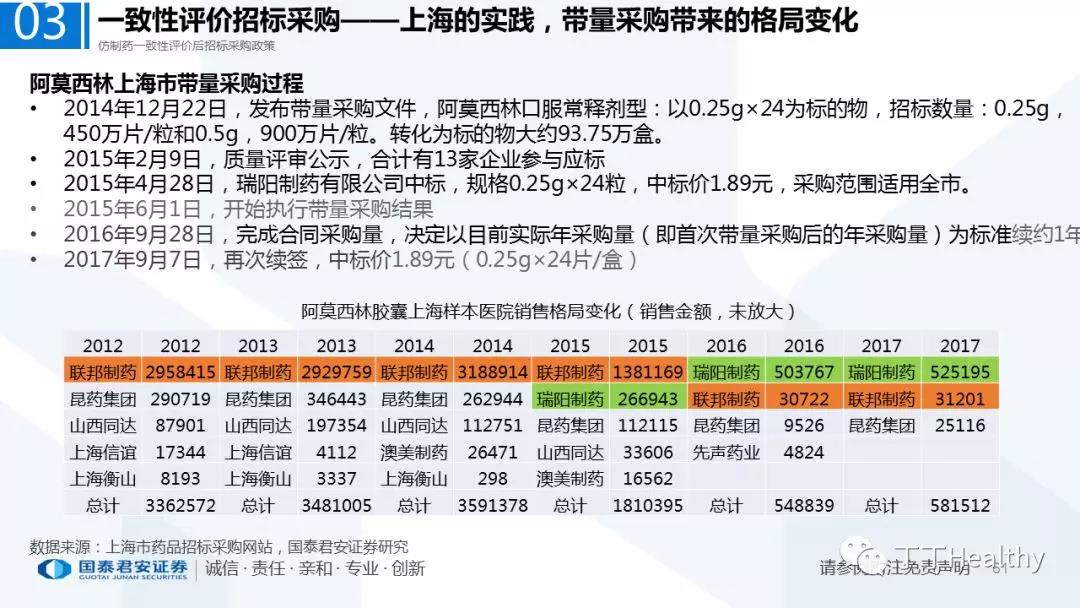
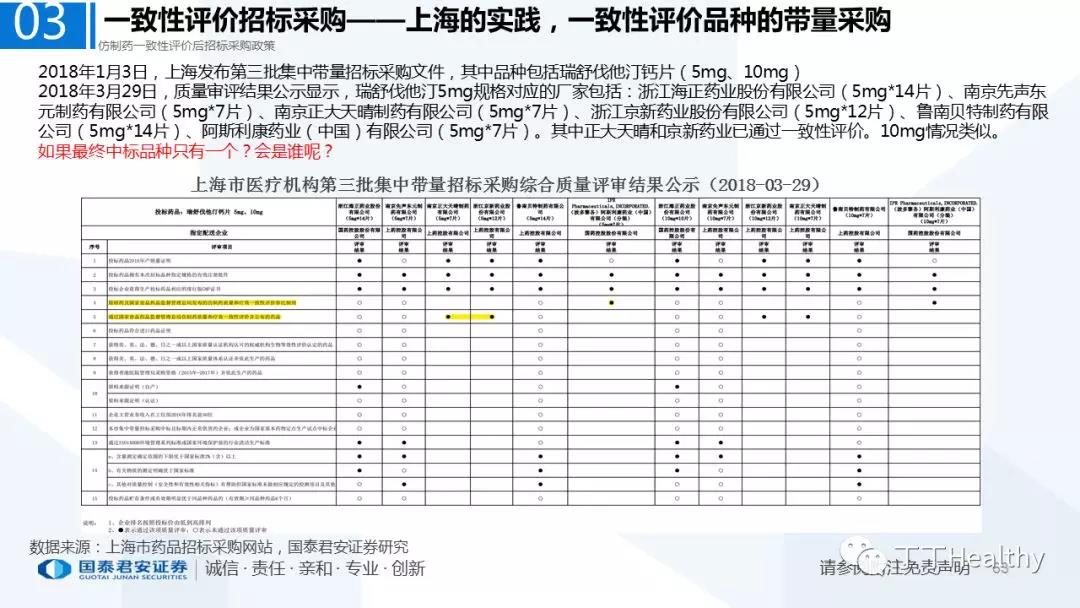
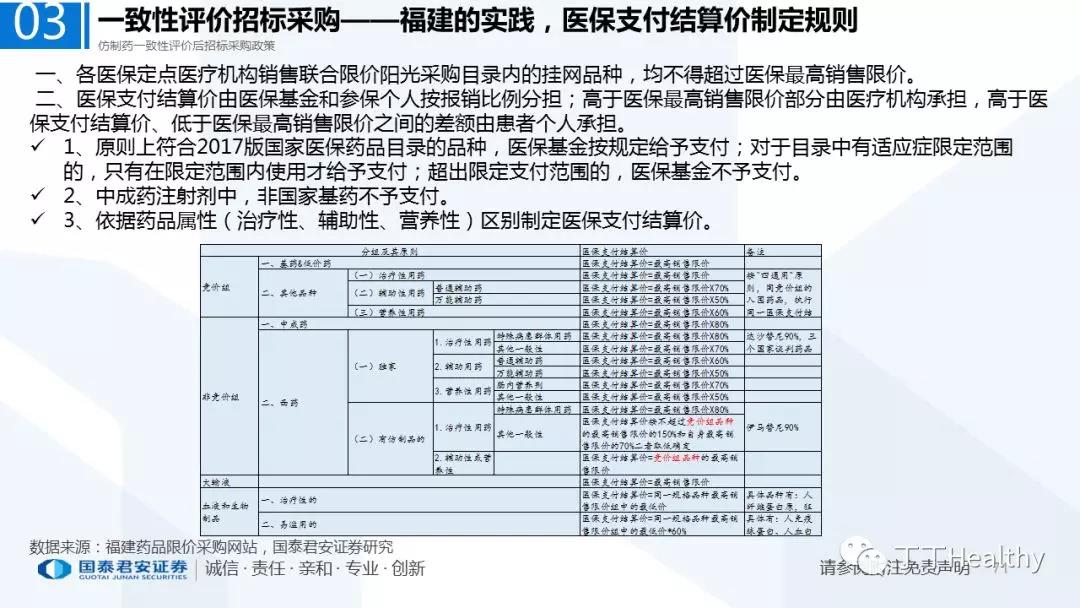
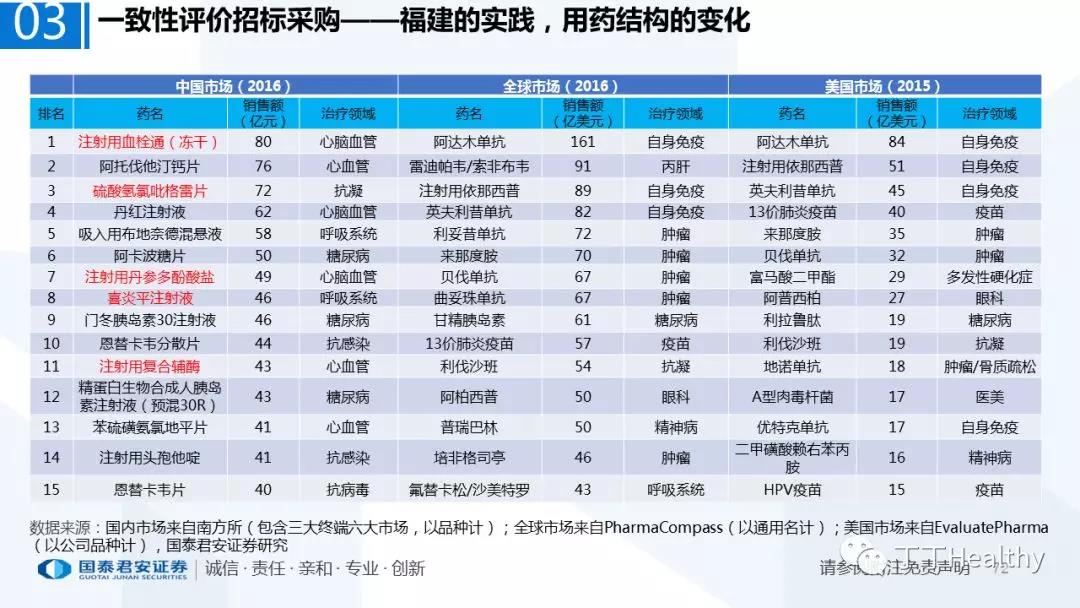
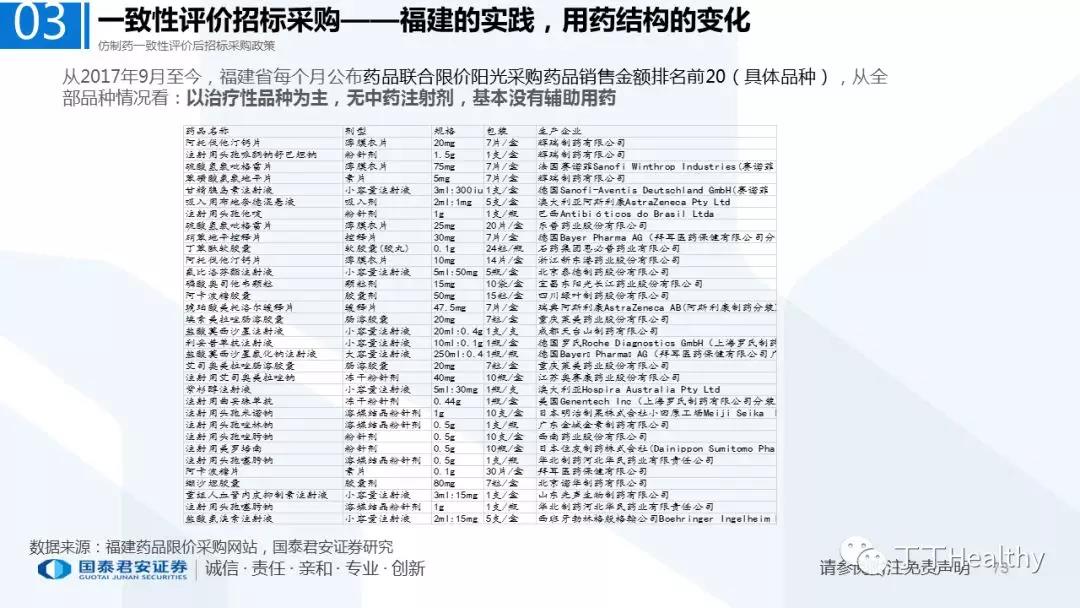
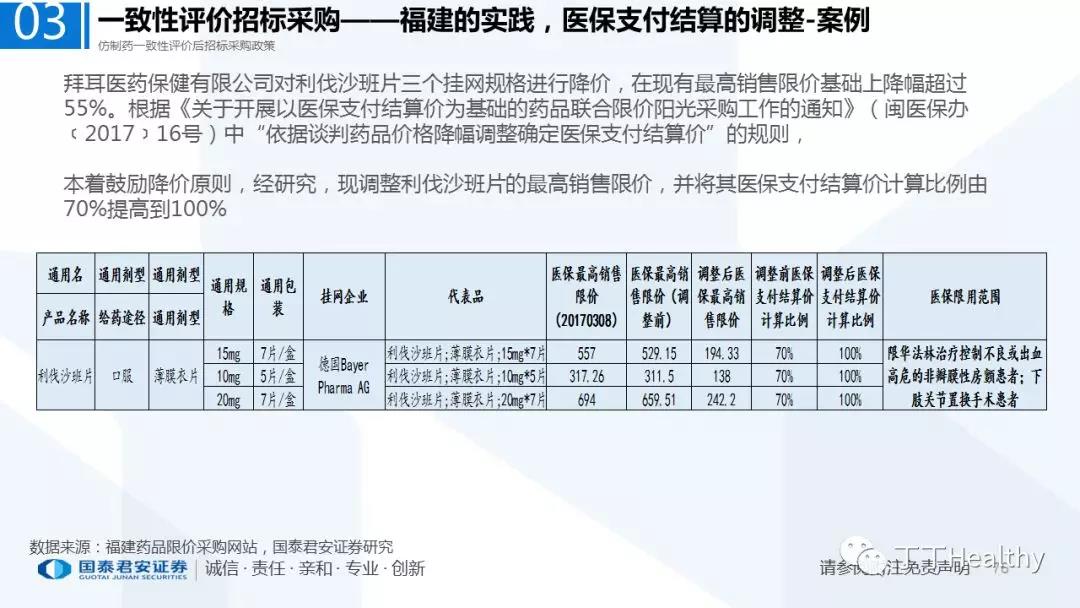
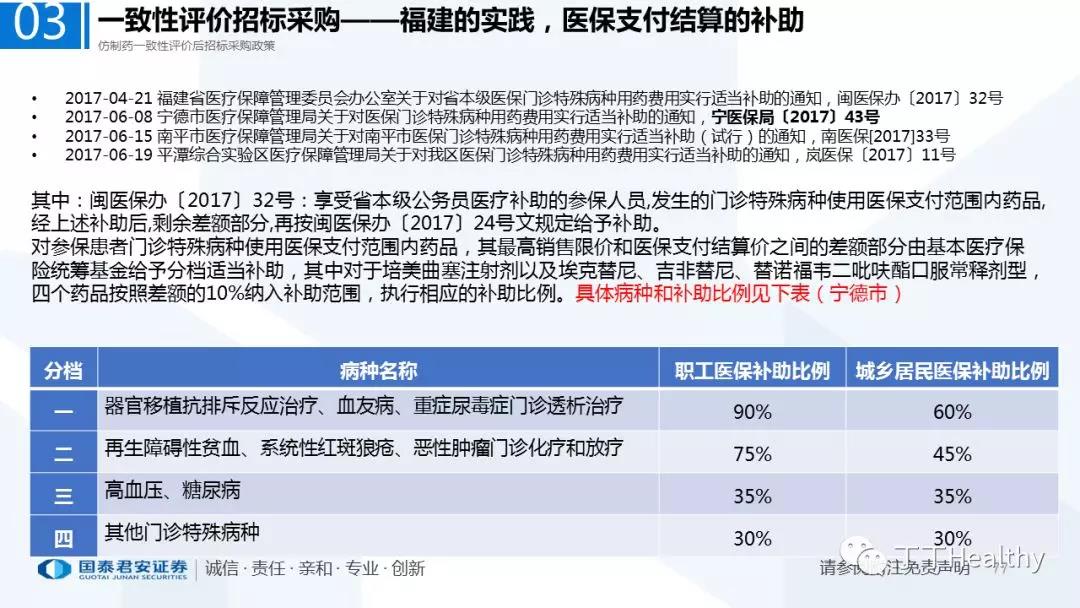
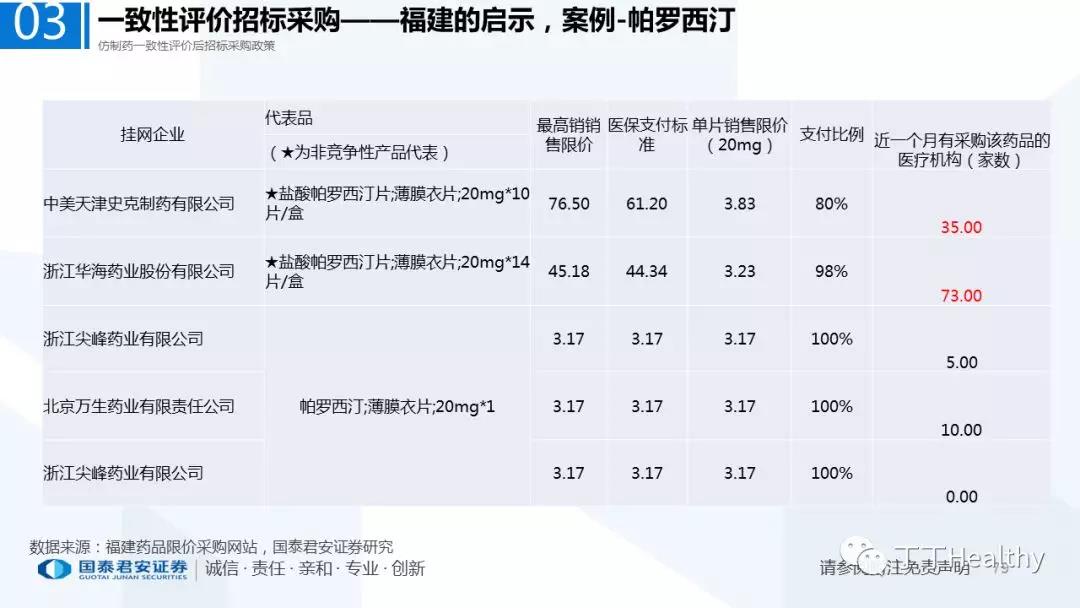
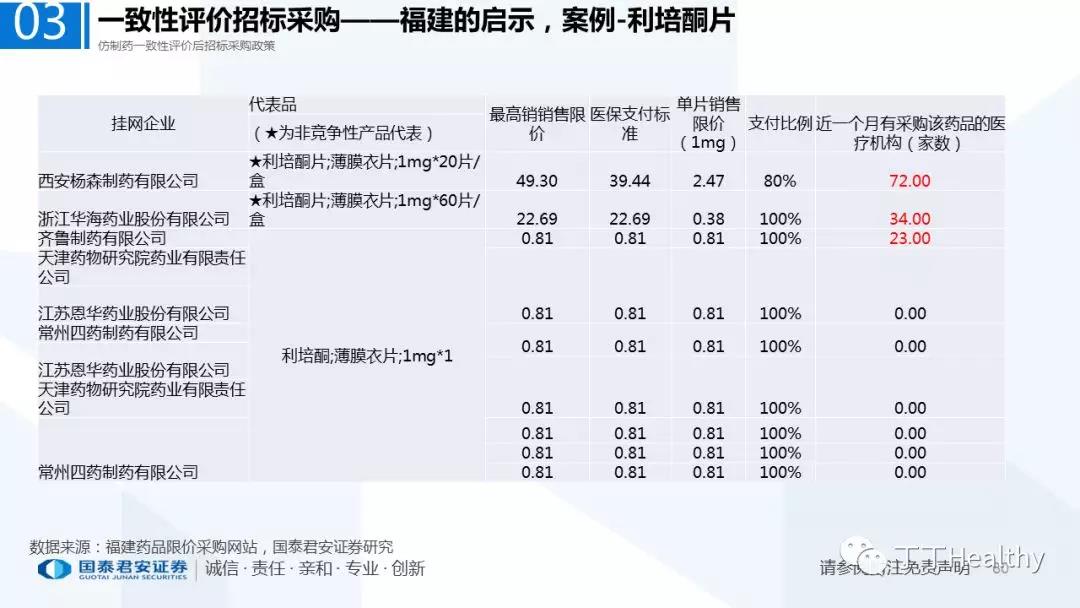
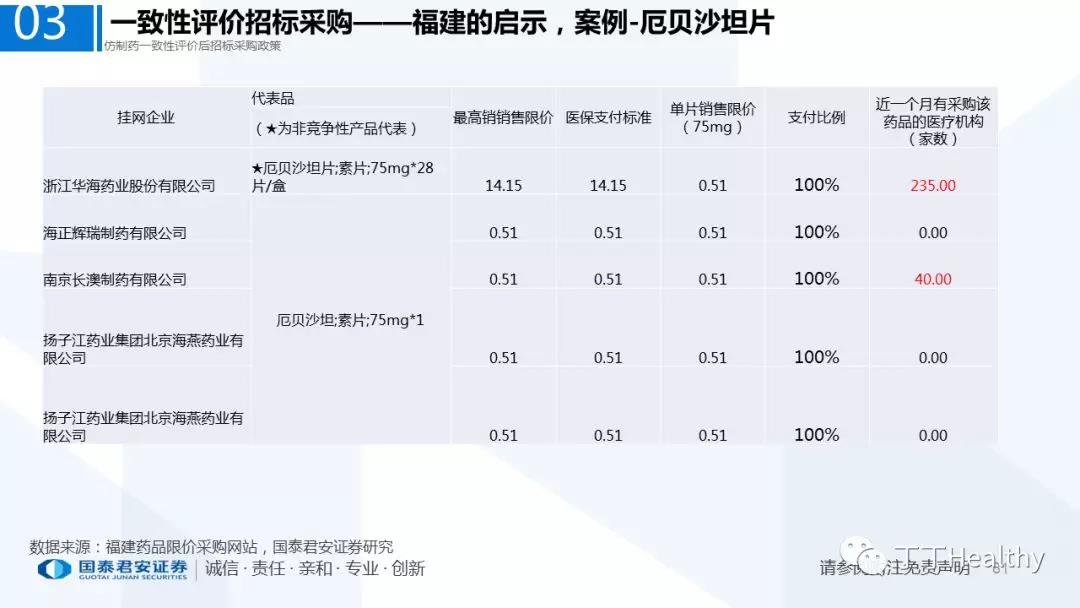
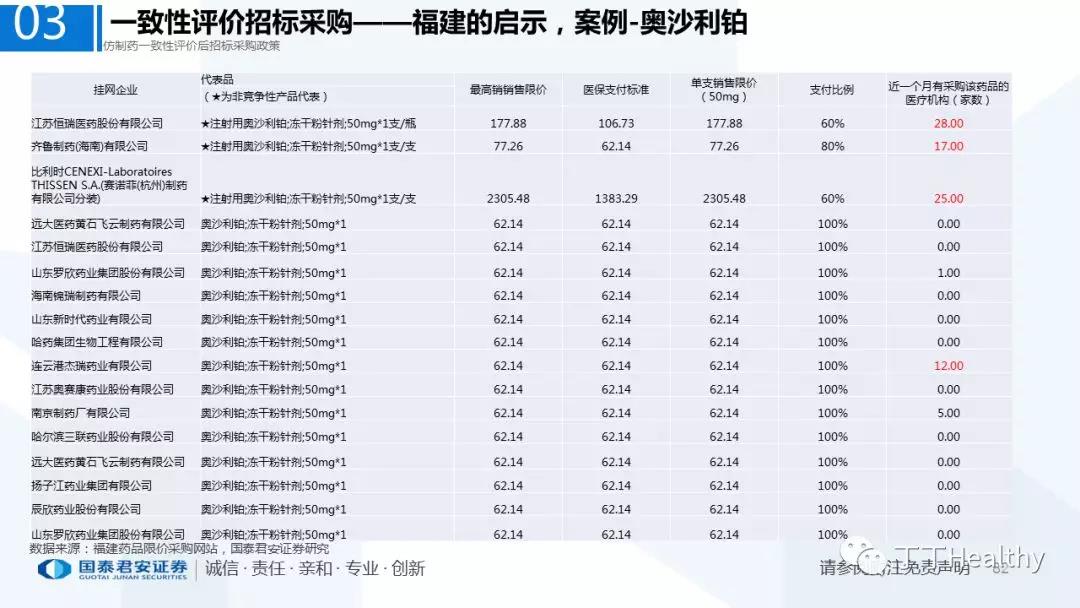
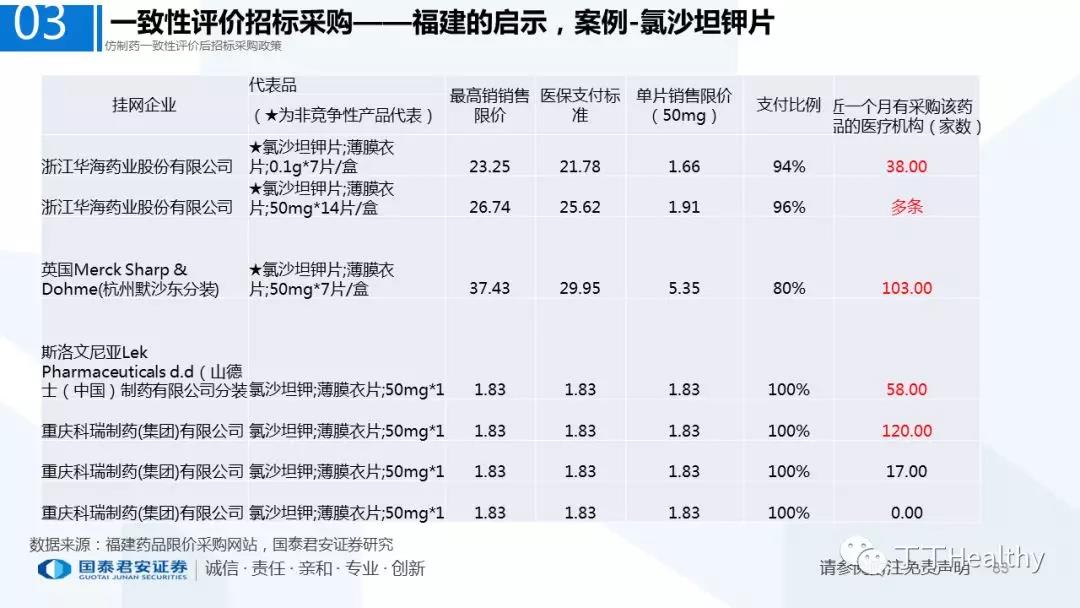
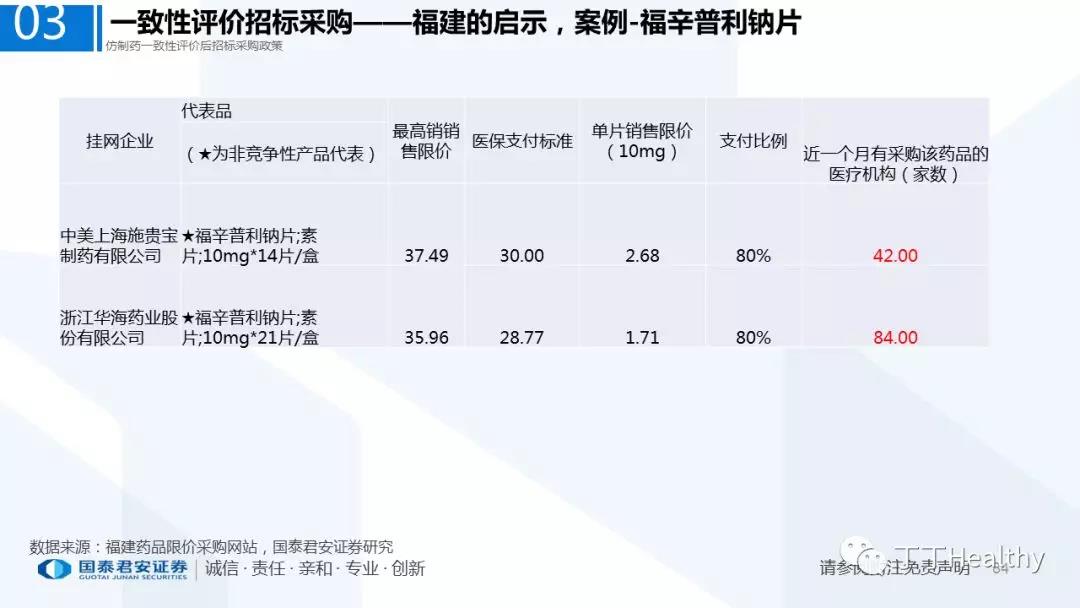
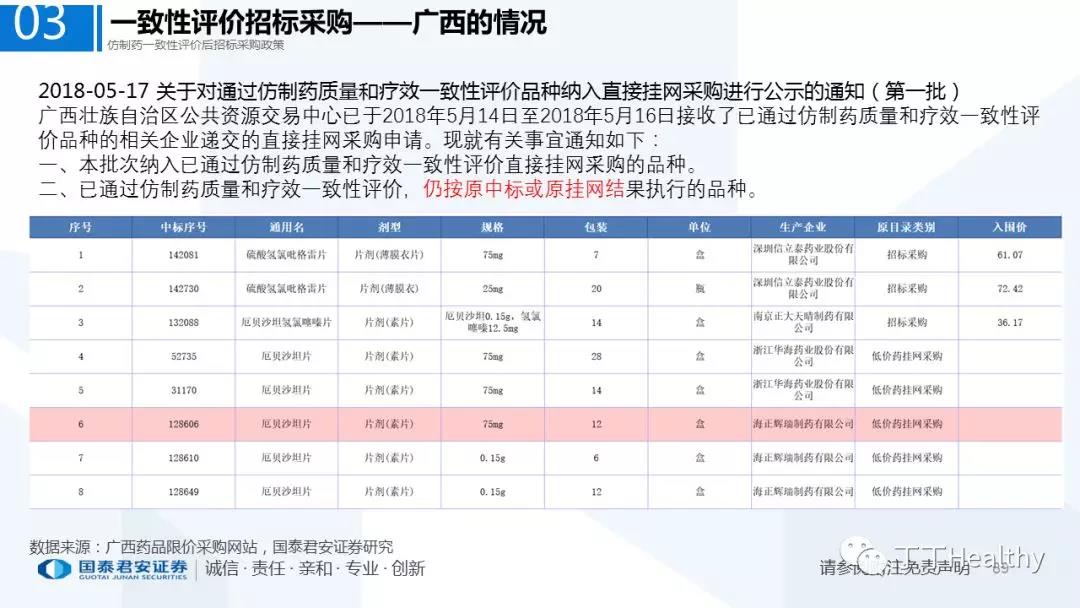
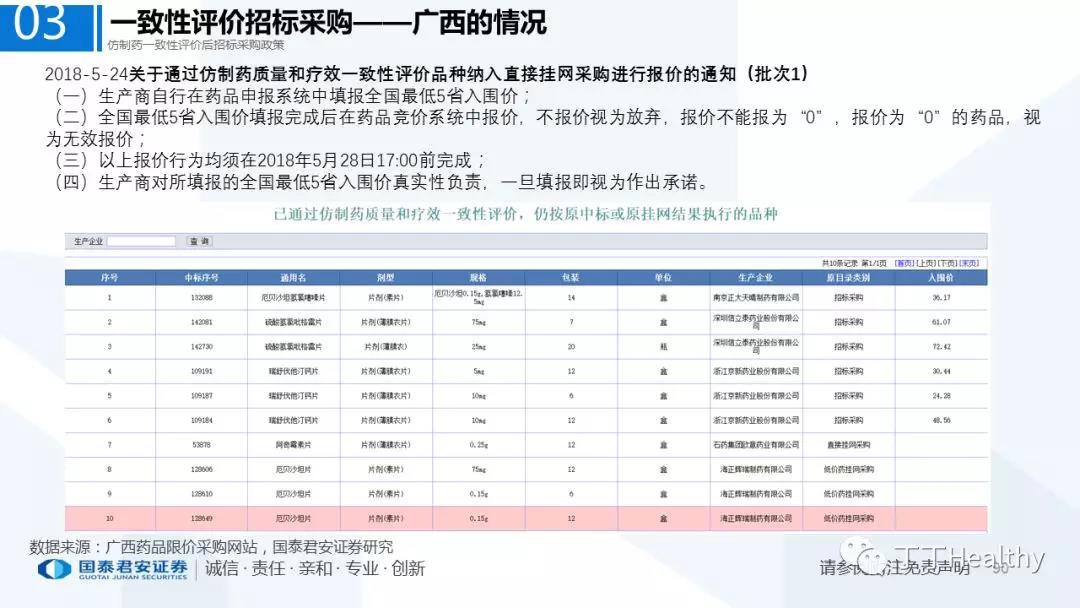
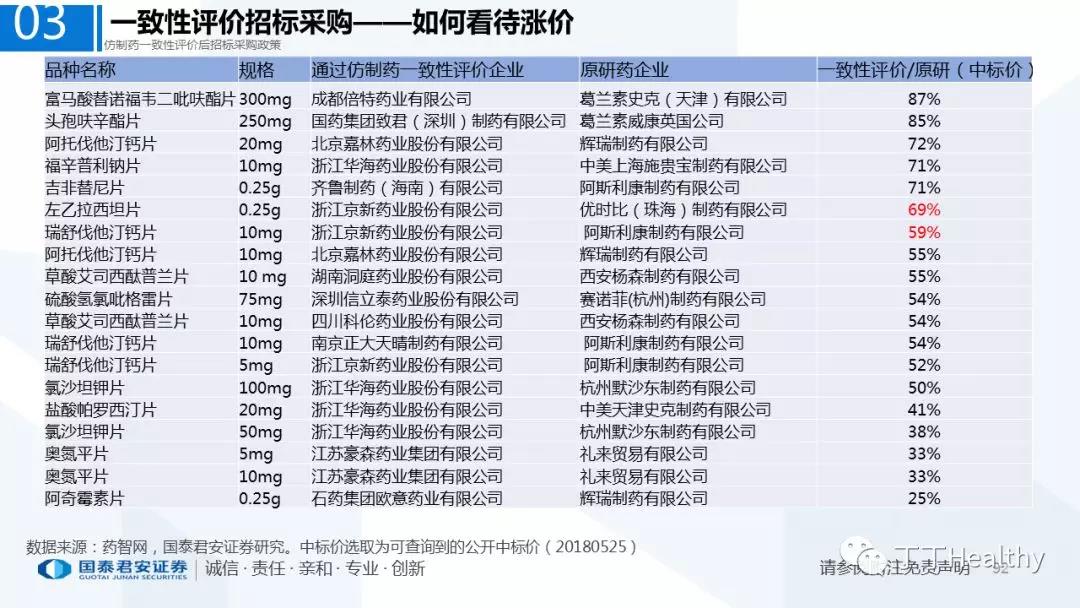
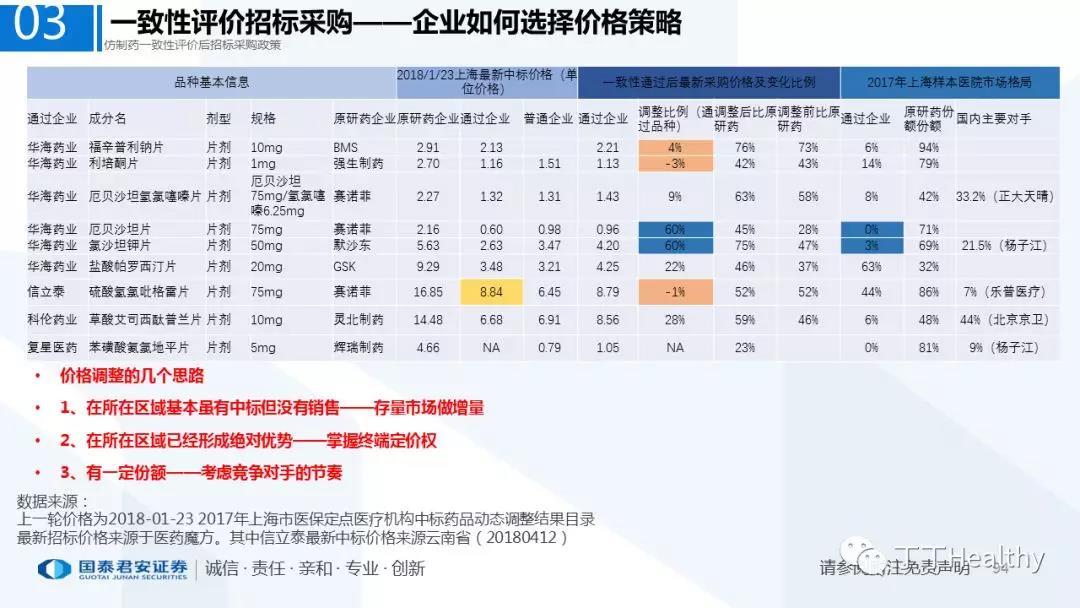
2.配套政策陆续落地,地方配套政策值得重点关注
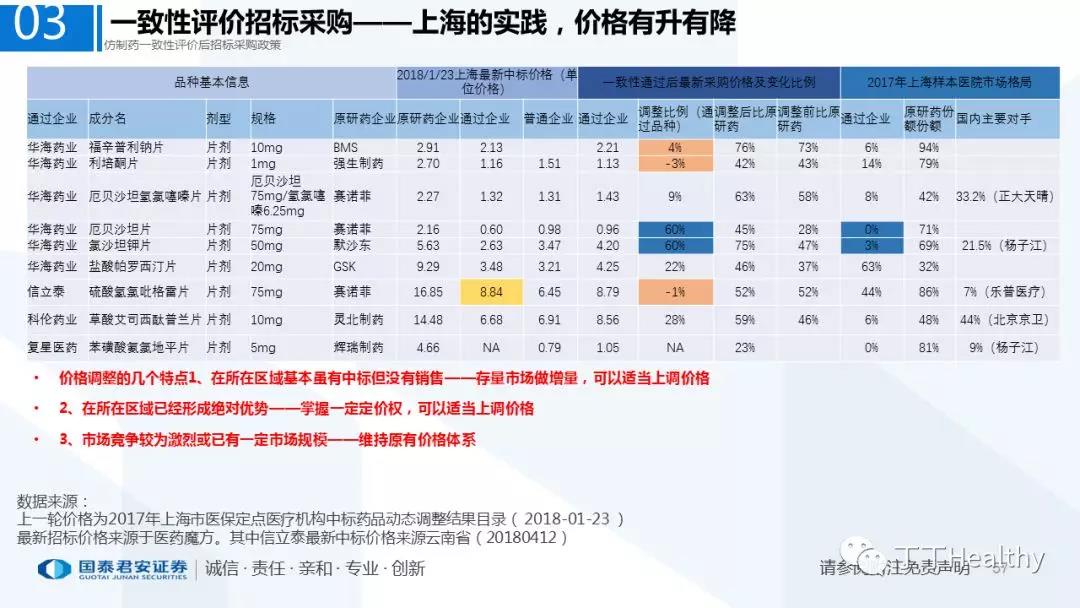
2018年至今已有至少11省份出台针对通过仿制药一致性评价的品种配套支持政策,包括招标采购、医保报销、使用等环节。地方鼓励政策的力度和进度都好于年初市场预期(尤其是上海、浙江等省份),如未来各地落地执行顺利,将对已通过品种带来积极影响。我们预计随着获批品种的增多,下半年将会有更多配套政策落地,为未来相关公司的产品放量构筑政策保障。
3.长周期新起点,一致性评价主题持续演绎
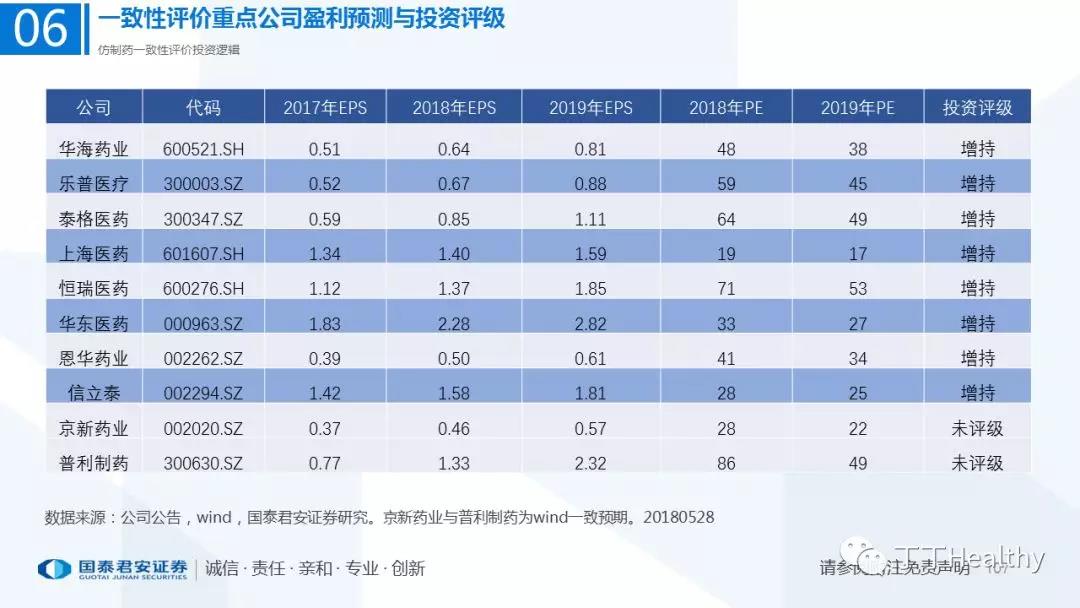
我们在2018年度医药行业投资策略报告中前瞻性判断:制药行业进入长周期新起点。工业基础扎实、有一定的利润体量、品种数量较多、重视一致性评价且进展顺利的优秀治疗型品种制药企业最终会受益于行业变革的结构性机会。维持重点制剂公司增持评级:华海药业、乐普医疗、泰格医药、恒瑞医药、上海医药、华东医药、信立泰、恩华药业;受益标的:普利制药。受益于行业回暖及BE试验需求强劲维持,维持CRO龙头泰格医药增持评级。
部分关键报告内容




 报告正文
报告正文































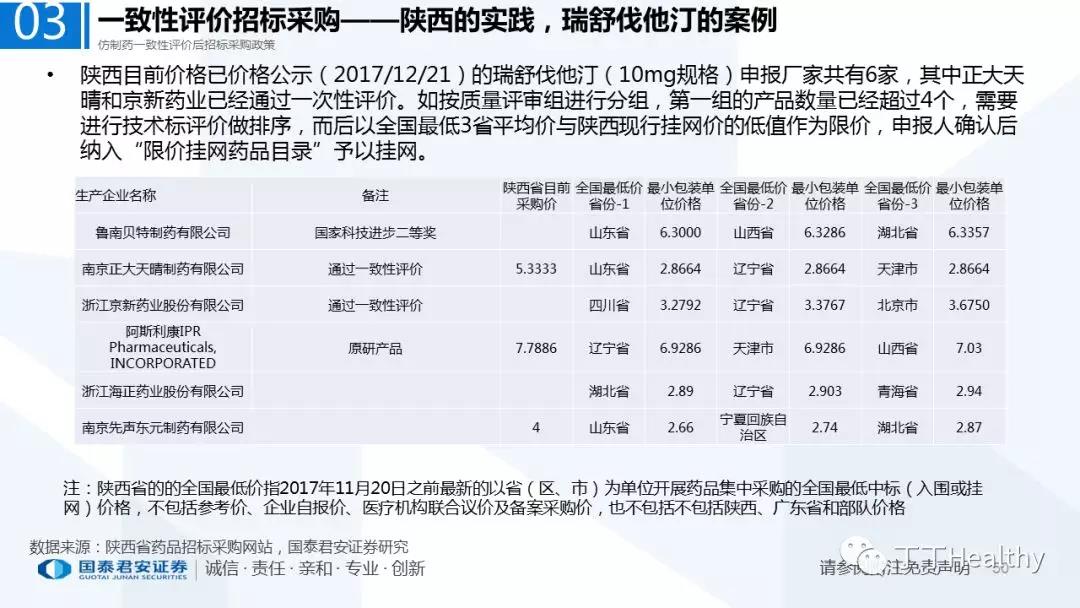



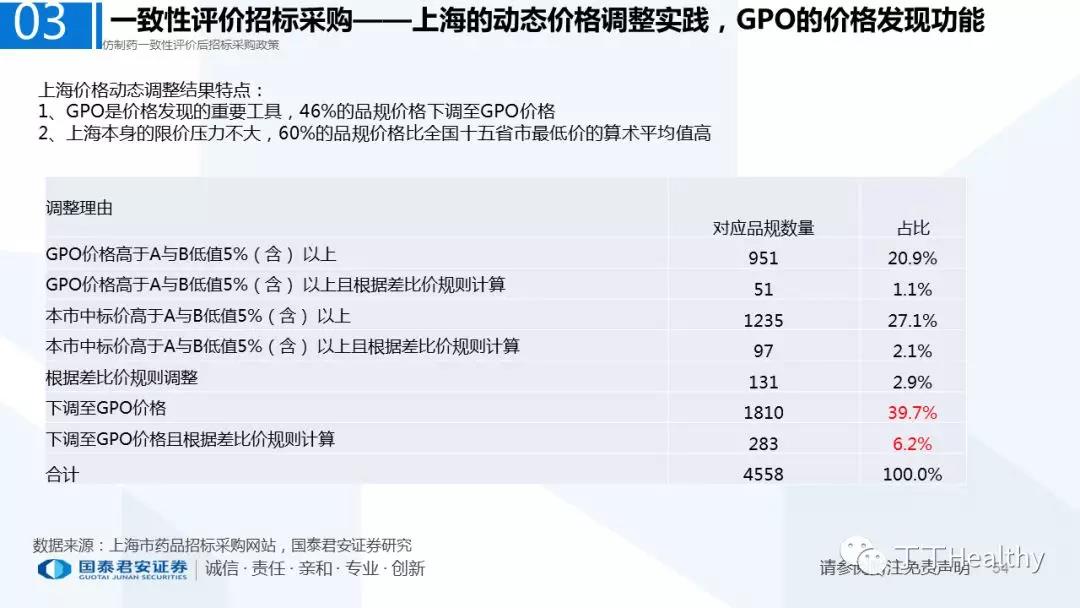
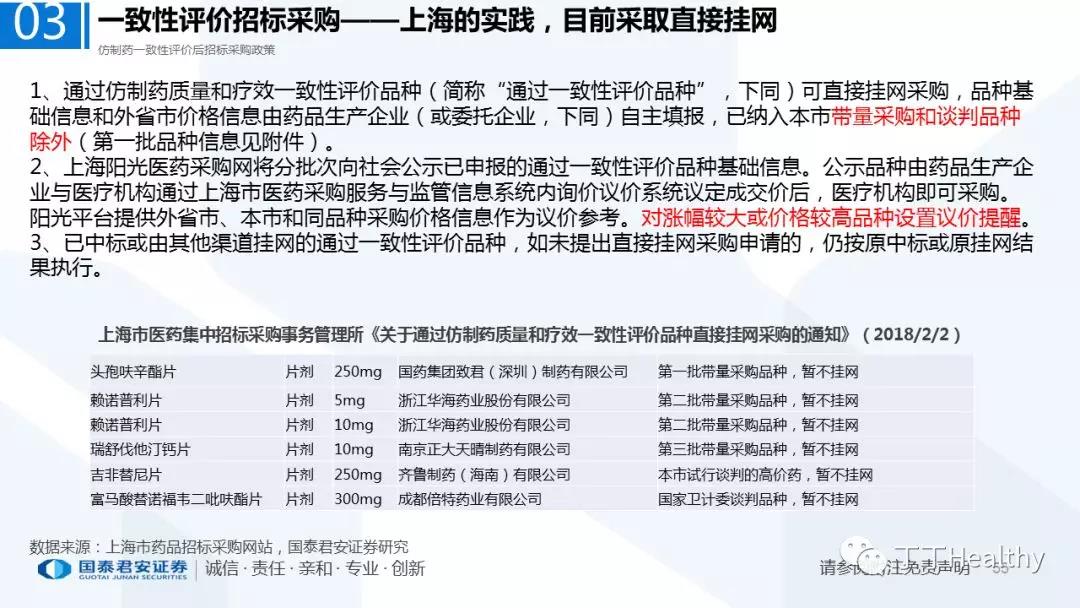
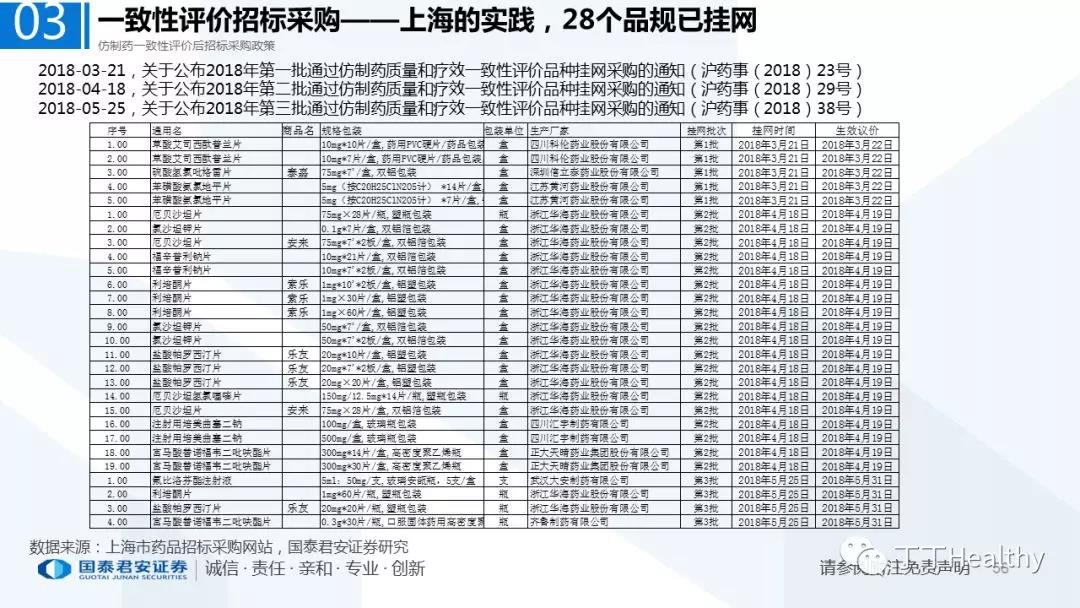



























【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx