今天,Janssen-Cilag International NV公司宣布含有darunavir成分的在研单片方案(STR)有效且耐受性良好。一项名为EMERALD的关键性3期研究结果表明,每日一次STR(darunavir 800 mg、cobicistat 150 mg、emtricitabine 200 mg和tenofovir alafenamide 10 mg,[D/C/F/TAF])治疗病毒抑制的HIV-1阳性成人患者具有良好功效。他们从标准增强蛋白酶抑制剂(PI)方案切换,在第24周时呈现了累积病毒反弹率低、病毒学抑制率高的治疗优势。
基于darunavir成分的STR在本月早些时候从欧盟药品管理局(EMA)的药物产品委员会(CHMP)获得了积极意见,建议在欧盟以品牌名称Symtuza上市。如果获得批准,这将是针对成人和青少年(12岁及以上,体重至少为40kg,具有基因型检测指导用途)治疗HIV-1的第一个darunavir完整组合方案。
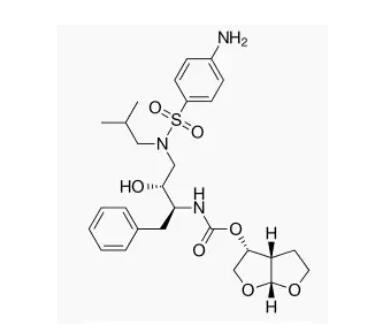
▲Darunavir的分子式(图片来源:Wikipedia)
EMERALD是一项为期48周的非劣效性研究,评估切换到D/C/F/TAF方案(n=763)与继续使用PI加F/TDF方案(n=378)相比较的疗效和安全性。累积病毒学反弹定义为确定的病毒载量(VL)=50c/mL或过早中断。最近的VL测量值为50c/mL,在D/C/F/TAF方案中为1.8%(n= 14),对照组为2.1%(n=8),在第24周时分别有10/14和5/8的病人得到抑制(<50c/mL),并且没有确认的反弹(VL=200c/mL)。在第24周,定义为VL<50c/mL的病毒学抑制率分别为96.3%(D/C/F/TAF组)和95.5%(对照组),没有检测到任何在研药物的耐药性。
Janssen传染病治疗科全球治疗领域负责人Lawrence M. Blatt博士说道:“过去十年里,Janssen为HIV病毒感染者开发了广泛的治疗方法,帮助改变患者病情管理。Darunavir是全世界范围内应用最广泛的HIV病毒 药物之一,它具有很高的遗传屏障,不产生耐药抗性。我们仍然致力于履行我们的转型创新宗旨,以满足HIV病毒感染群体的多样化需求,并很高兴以darunavir为骨干推出一种不断进步的新疗法。如果获得批准,它不仅可以提供darunavir的疗效益处,而且还可以减少终身服用HIV病毒 药物的治疗负担,可能有助于解决依从性和耐药性难题。”
参考资料:
[1] Janssen-Cilag International NV (JNJ) Announces Phase III Pivotal Study Results for Darunavir-Based Complete Treatment Regimen
[2] Janssen-Cilag International NV官方网站
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx