2月13日,CFDA官网发布了<关于药械组合产品属性界定结果的公告>,将2009年以来的药械组合产品属性界定结果予以公告(形成界定意见的有85件,获得批准上市的有4件),旨在引导申请人合理申报。
根据2009年CFDA发布的<关于药械组合产品注册有关事宜的通告>,以药品作用为主的药械组合产品,需申报药品注册;以医疗器械作用为主的药械组合产品,需申报医疗器械注册。
表1 药械组合产品属性界定结果汇总
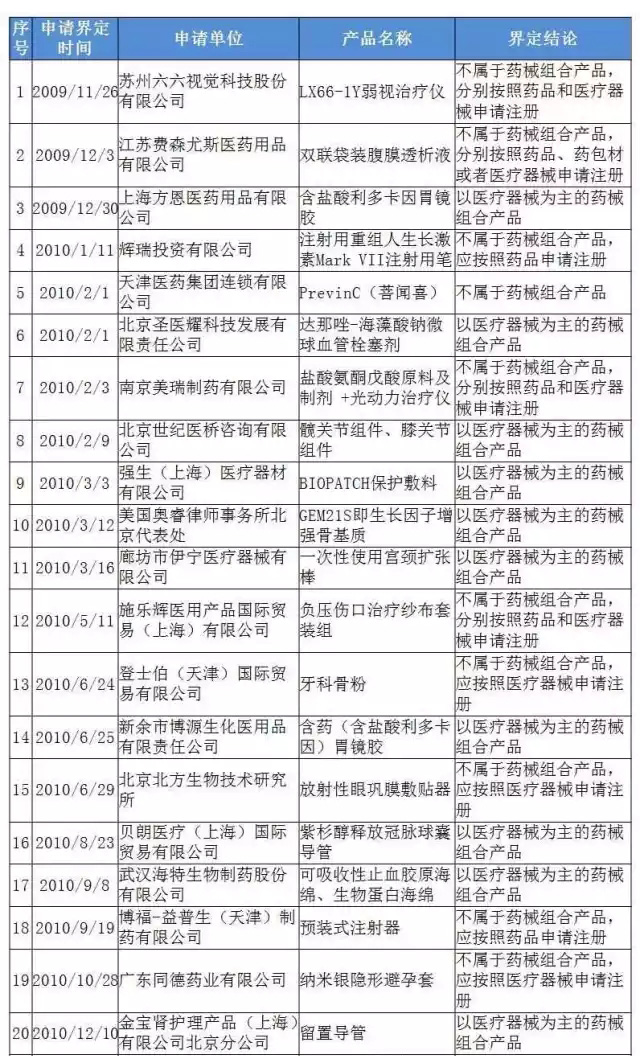
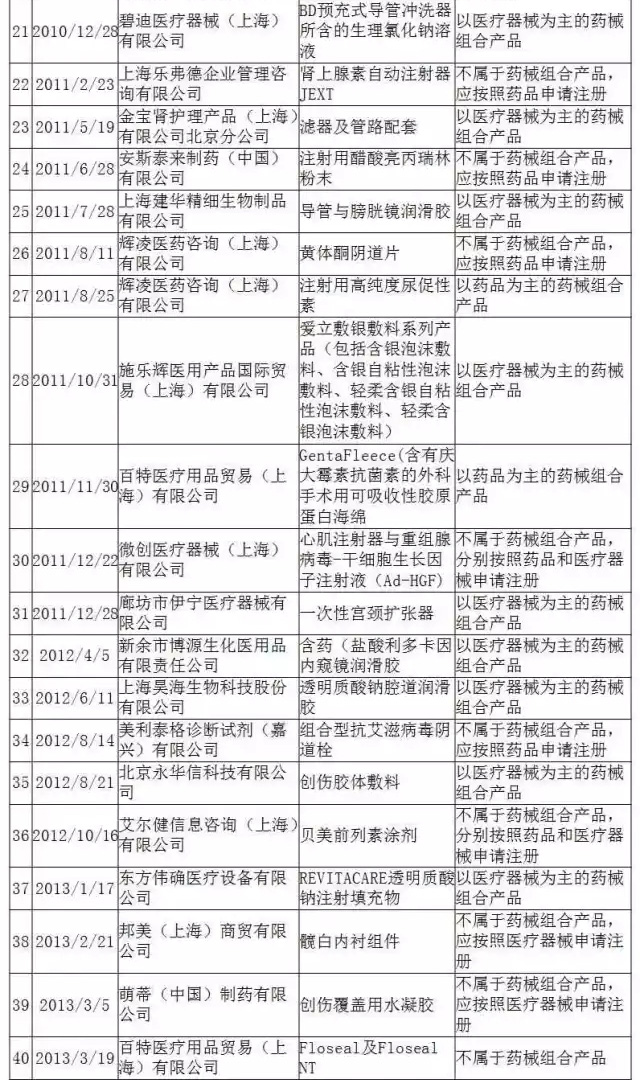
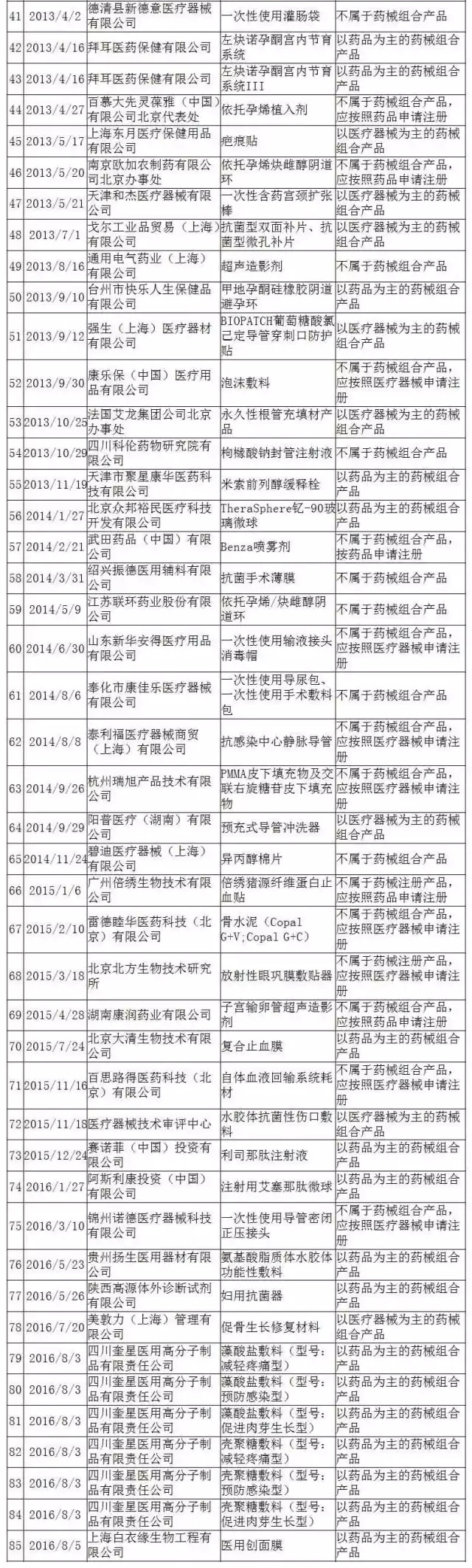
表2 批准上市的药械组合产品名单
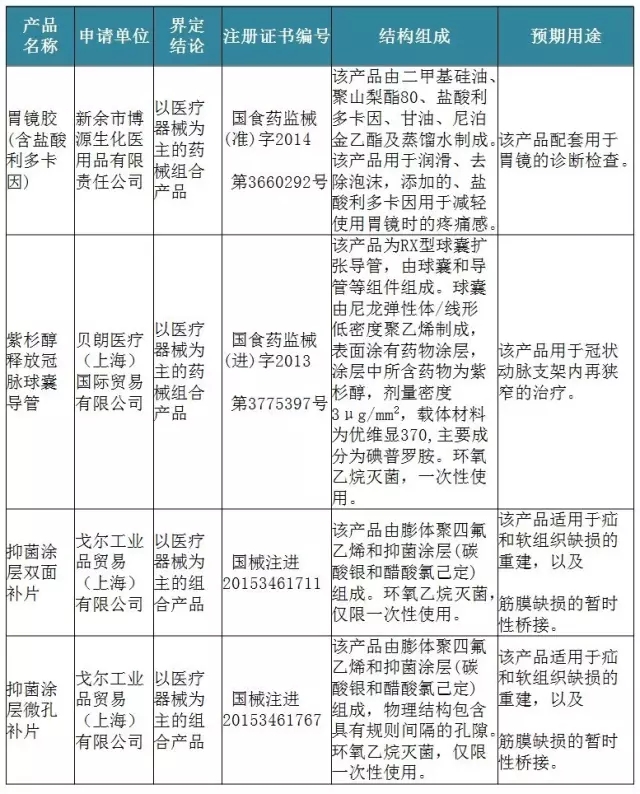
■来源/CFDA官网
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx