笔者查询咸达药海数据发现,2025年,有不少关于原研厂家地产化产品,如西安杨森的复方角菜酸酯栓和复方角菜酸酯乳膏、进口仿制药(含地产化产品)和进口原研产品(含进口分包装产品)依申请注销的信息。
目前来看,原研产品(含地产化和进口产品)选择在国内退市,通常有五大原因:一是原料难以获得;二是政策调控产品停产;三是品牌收购/授权后退市;四是仿制药/同靶点厂家竞争激烈;五是商业化未成功。那么原研品种退出后,相关品类的市场竞争格局如何?本文试以代表品种为例作简要分析。
无替代品
注销原因:原料断供
代表品:西安杨森的复方角菜酸酯栓和复方角菜酸酯乳膏
2023年以前,作为孕妇也能安心使用的独家治疗痔疮药,西安杨森的复方角菜酸酯栓和复方角菜酸酯乳膏产品在国内市场能维持过亿元的销售额。
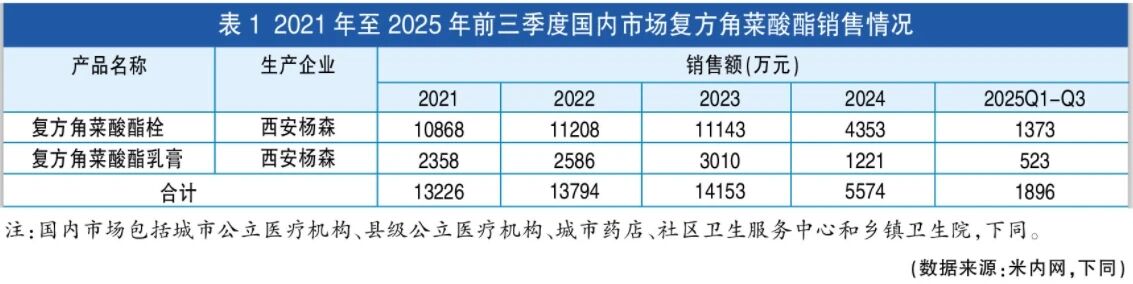
复方角菜酸酯是从爱尔兰红藻纲海藻(红色海藻)中提取获得,基于该原材料天然提取且不可再生,目前全球已无原料可持续供应生产。自2023年11月起,西安杨森停止复方角菜酸酯栓的供应,并于2023年10月向国家药监局递交撤市申请。
定点生产
注销原因:管控停产
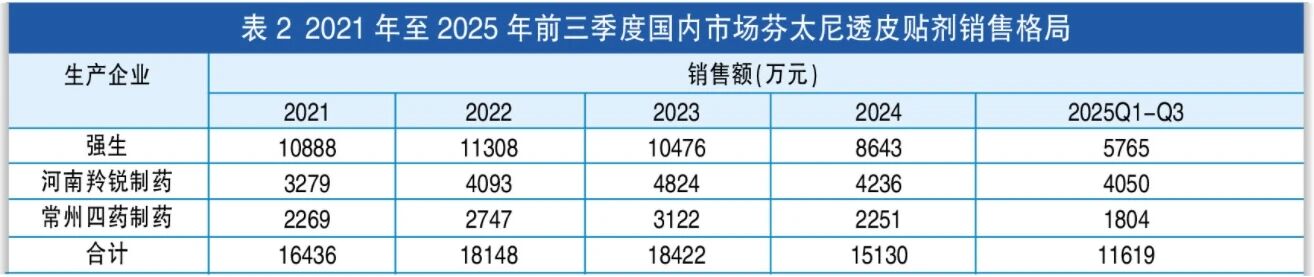
代表品:强生的芬太尼透皮贴剂(包括以下6个规格:12微克/小时,2.1mg/贴;25微克/小时,4.2mg/贴;75微克/小时,12.6mg/贴;50微克/小时,8.4mg/贴;25微克/小时,4.2mg/贴;50微克/小时,8.4mg/贴)
2025年12月,美国收紧合成阿片类止痛剂芬太尼的政策。此前,美国已采取多种措施限制芬太尼的生产和商业流通,强生也因此调整全球商业及供应链策略,停止生产和销售芬太尼透皮贴剂。西安杨森从比利时进口强生的芬太尼透皮贴剂,自2025年4月起停止向中国供应,库存售罄后退出国内市场,于2025年4月15日向国家药监局提交退市申请(药品注册证有效期至2025年9月16日)。
在国内,芬太尼透皮贴剂的市场销售额峰值为2023年的1.8亿元。强生的芬太尼透皮贴剂退市后,预计市场将由河南羚锐制药和常州四药制药瓜分。2025年3月,国务院新闻办公室发布《中国的芬太尼类物质管控》白皮书。目前,中国共批准5家芬太尼类药品定点生产企业,预计未来不会新增定点生产企业,也不会批准进口产品。这意味着该产品将不会有新的仿制药获批上市。
品牌焕新
注销原因:品牌收购/授权
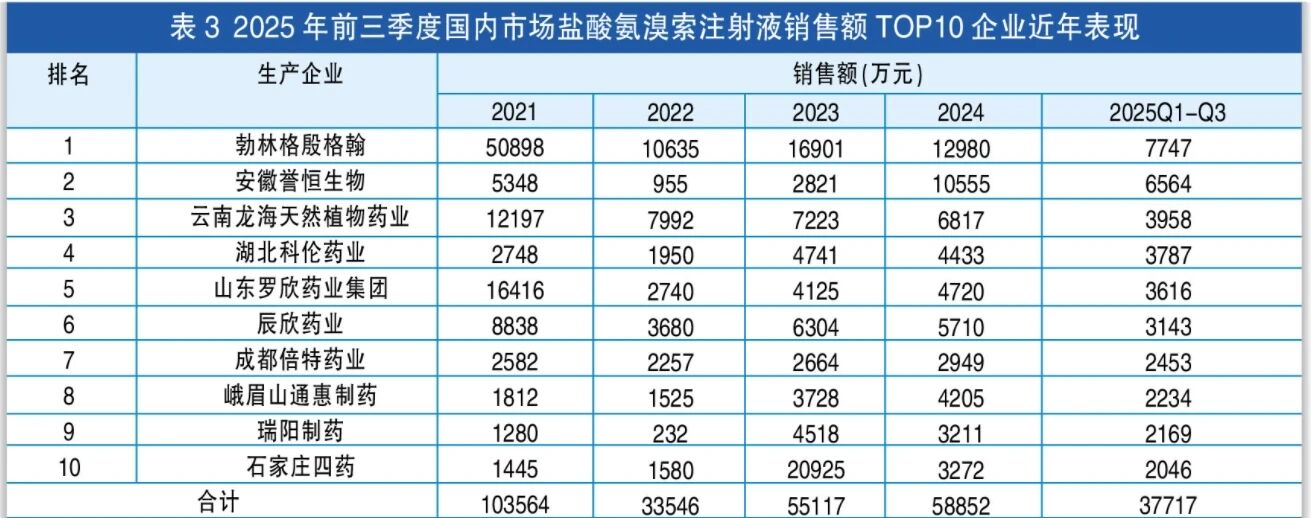
代表品:勃林格殷格翰的氨溴索注射液
2018年1月起,勃林格殷格翰将旗下呼吸系统类产品氨溴索注射液(商品名“沐舒坦”)在中国的推广独家授权给浙江医学科技开发有限公司。该产品的注册证于2020年到期但未再注册。此后,原研企业勃林格殷格翰中国发布公告称,无法持续为中国市场供应氨溴索注射液,将在2024年一季度停止业务。米内网数据显示,2024年,盐酸氨溴索注射液国内市场销售额超过8亿元,勃林格殷格翰的产品销售额排名第一。
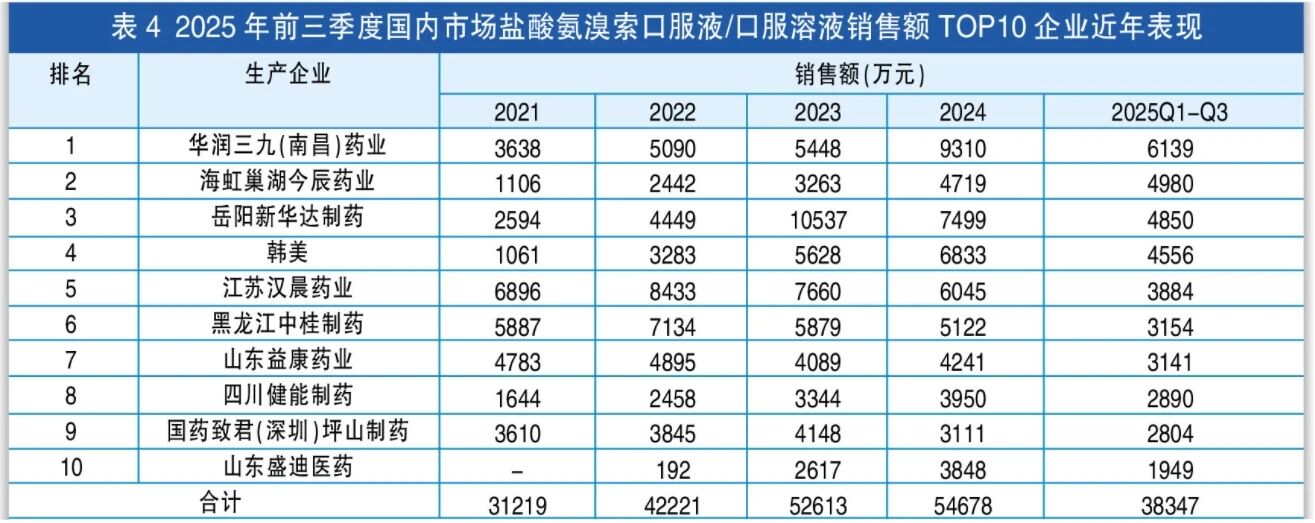
2025年,欧彼乐公布旗下原研品牌沐舒坦(盐酸氨溴索口服溶液)经过四年的重新注册流程,计划于2025年12月重返中国市场。2026年1月,产品已经登陆部分线下渠道。早在2016年,赛诺菲的动物保健业务和勃林格殷格翰的消费者保健业务互换,勃林格殷格翰拿到了赛诺菲的动物保健业务,而赛诺菲则收获了勃林格殷格翰的消费者保健业务,此次重新上市的沐舒坦生产企业欧彼乐就是赛诺菲的子公司。
米内网数据显示,2024年,盐酸氨溴索口服溶液国内市场销售额接近9亿元,目前销售额最高的产品来自华润三九,2024年销售额近亿元,原研厂家再出发,能抢到多少市场,值得期待。
集采分羹
注销原因:仿制药/同靶点厂家竞争激烈
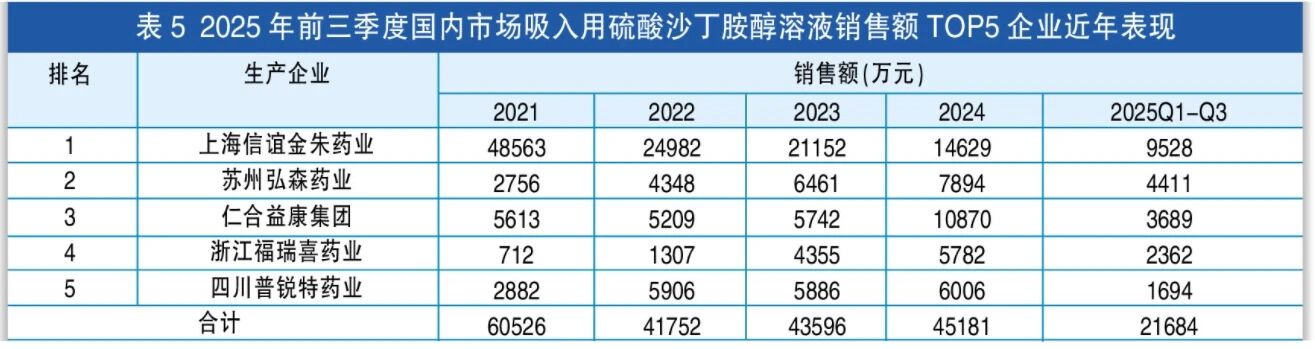
代表品:葛兰素史克的吸入用硫酸沙丁胺醇溶液
吸入用硫酸沙丁胺醇溶液被纳入第四批国采,按2025年前三季度销售额排行前十企业,2021年国内市场销售额合计达7.2亿元,2024年回升至4.8亿元。医院渠道为主的产品,若集采不中标,基本很难在院外有所作为。葛兰素史克的产品从2019年销售峰值的2.7亿元降至近年的千万元规模,退市也在意料之中。
转换赛道
注销原因:商业化未成功
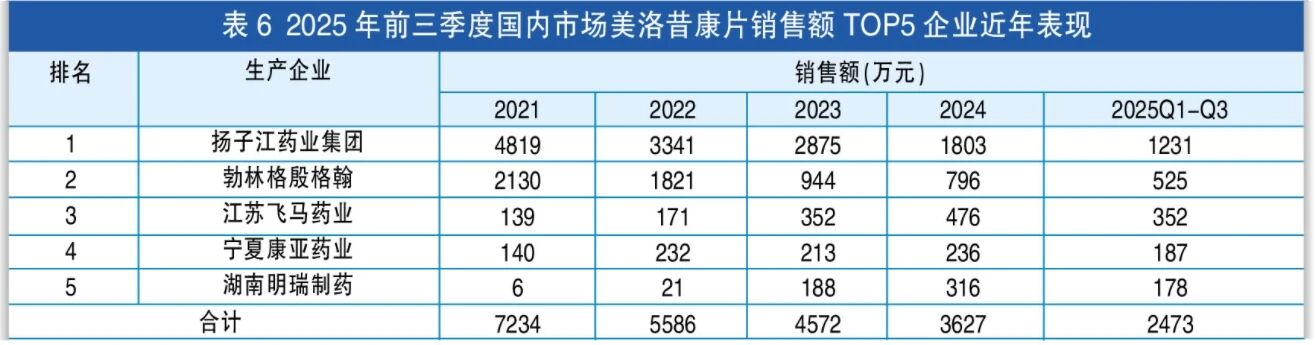
代表品:勃林格殷格翰的美洛昔康注射液
根据米内网数据,2021年美洛昔康注射液销售额达到峰值,为73万元,此后基本不再销售。美洛昔康注射液之所以未能成功商业化,本质上还是因为产品缺陷。该产品的给药途径为肌肉注射,但无法快速起效,且使用的辅料有刺激性和毒性,存在一定的安全性问题,已在美国退市。虽然该产品曾在国内产生销售数据,但我国仿制药参比制剂目录仍采用未进口的原研药品。
美洛昔康的畅销剂型为片剂,2020年以前,国内年销售额超过4亿元;纳入第二批国采后,2020年销售额不足2亿元,随后逐年下滑,2024年销售额降至4166万元。目前,国内年销售额最高的产品来自扬子江,其次是原研产品。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx