药捷安康宣布达成一项超8亿美元授权合作
11月3日,药捷安康(南京)科技股份有限公司发布公告宣布,公司与Neurocrine Biosciences, Inc.订立一项付特许权使用费的专利转让及研究合作协议,以开发NLRP3抑制剂,用于治疗多种疾病。
 截图来源:药捷安康公告
截图来源:药捷安康公告
根据该协议,Neurocrine获授予在大中华区以外开发、制造及商业化药捷安康NLRP3药物平台中的NLRP3抑制剂的独家权利,药捷安康拥有在大中华区(内地、 香港、台湾、澳门)开发、制造及商业化NLRP3抑制剂的权利。
协议显示,药捷安康将有权获得预付款,并且根据Neurocrine的开发和商业化进展,可能会收到与研发里程碑和销售里程碑相关的进一步里程碑付款,该协议的总潜在价值为 8.815亿美元,且进一步涵盖订约方之间的研究合作,以进一步发展NLRP3相关技术。
辉瑞启动PD1/VEGF双抗两项Ⅲ期临床
公开资料显示,PF-08634404是三生制药开发的一款PD1/VEGF 双抗,2025年5月,辉瑞以 60.5亿美元引进该产品全球权益,其中首付款高达12.5亿美元,创中国创新药出海新纪录。
此次辉瑞启动的针对非小细胞肺癌的Ⅲ期研究,是一项随机、双盲、干预性Ⅲ期临床研究,旨在评估PF-08634404联合化疗与帕博利珠单抗联合化疗治疗局部晚期或转移性非小细胞肺癌成年患者的疗效和安全性。
 截图来源:ClinicalTrials.gov官网
截图来源:ClinicalTrials.gov官网
该研究计划入组1500 名受试者,随机分配接受PF-08634404+化疗和帕博利珠单抗+化疗治疗。
 截图来源:ClinicalTrials.gov官网
截图来源:ClinicalTrials.gov官网
研究主要终点是总生存期(OS)和由BICR评估的无进展生存期(PFS),次要终点包括客观缓解率(ORR)、缓解持续时间(DOR)研究者评估的PFS等。
东阳光药抗乙肝siRNA新药获批临床
11月1日,国家药品监督管理局药品审评中心(CDE)官网最新公开显示,东阳光药申报的1类新药HECN30227获批临床,拟定适应症为慢性乙型肝炎。根据东阳光药公开资料,这是其自主研发的siRNA疗法。
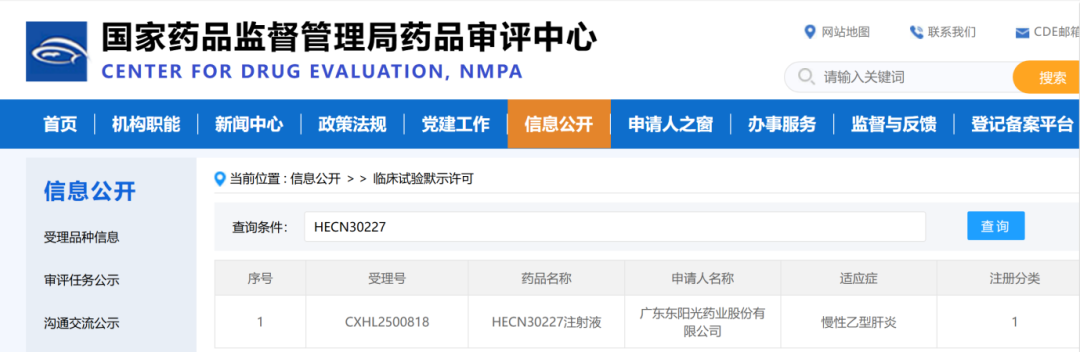 截图来源:CDE官网
截图来源:CDE官网
据介绍,HECN30227是东阳光药基于小核酸技术平台开发的首款siRNA药物,可同时消除cccDNA和intDNA来源的乙肝表面抗原(HBsAg)。临床前数据表明,该产品具有泛基因型活性,可高效降低HBsAg水平,对核苷类药物耐药株同样保持突出药效。该药物采用东阳光药自主设计的HEC-GalNova(N-乙酰半乳糖胺)肝靶向递送系统,在实现精准高效肝脏递送的同时大幅降低脱靶风险。
此外,基于对HBV清除机制的深刻了解,东阳光药正同步开发“siRNA+ASO+免疫调节剂”三联疗法,通过多靶点协同作用全面抑制HBV和HBsAg,并通过免疫重建开启乙肝“功能性治愈”新时代。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx